PCR MOLGEN2
Module: MOLGEN2: DNA-analyse
Inhoud van deze module:
1.
2.
3.
4.
Wat is er nu bekend?
Wat kan je analyseren
Hoe kan je dat analyseren?
Analysetechnieken (overzichtje)
a.
b.
c.
DNA-isolatie
DNA-amplicficatie: PCR
Amplicon-detectie: gelectroforese
Module: PCR analyse en Gelelectroforese
1
PCR MOLGEN2
Bekend:
1. De DNA-volgorde van slechts enkele
soorten (Mens, fruitvlieg, kip, koe, worm
etc)
2. Van veel soorten is slechts een klein deel
bekend
3. Van productiegewassen en dieren is
inmiddels het gehele genoom wel bekend.
(Financieel belang)
4. Het kennen van de DNA-volgorde wil niet
zeggen dat je de genen kent!!!
Module: PCR analyse en Gelelectroforese
2
PCR MOLGEN2
Tools:
1.
Genbanken zoals ncbi:
http://www.ncbi.nlm.nih.gov/nuccore
2.
DNA-tools voor het maken van zogenaamde primers
(straks meer)
3.
Blasts: het opzoeken of stukken DNA-volgorde
ergens in het genoom voorkomen.
Hiermee wordt verwantschapsanalyse tussen
soorten gedaan
4.
Merkers en microsatellieten: Hiermee worden
vaderschaps-tests uitgevoerd. Voor een individue
kenmerkende sequenties.
Module: PCR analyse en Gelelectroforese
3
PCR MOLGEN2
Fruitvlieg
Nbci-database bevat genoom van veel organismen:
• Fruitvlieg chromosoom X:
http://www.ncbi.nlm.nih.gov/nuccore/667695275?report=graph
Fruitvlieg vg: Chromosoom 2R:
http://www.ncbi.nlm.nih.gov/nuccore/113194556?report=graph&tracks=[key:sequence_track,name:Sequence,d
isplay_name:Sequence,id:STD1,category:Sequence,annots:Sequence,ShowLabel:false][key:gene_model_track,n
ame:Genes,display_name:Genes,id:STD3,category:Genes,annots:Unnamed,Options:MergeAll,SNPs:false,CDSProd
uctFeats:false,ShowLabelsForAllFeatures:false,HighlightMode:2]&appname=ncbientreznuccore&color=0&label=0
&decor=0&spacing=0&v=8767788:8781704&c=333333&gflip=false&select=gi|113194556-0085e3f9-008611440103-8ca27e44-ffea8d58
Module: PCR analyse en Gelelectroforese
4
PCR MOLGEN2
DNA-analyse.
Hoe onderzoekt men of een gen er is?
1.
Je moet de sequentie van het gen kennen (uit eerder
onderzoek)
2.
3.
Je moet een idee hebben wáár het zit.
4.
We kiezen stukjes flankerende DNA-sequenties om de
aanwezigheid van dit gen te vinden:
Je zoekt in de ncbi-database die plek op.
Bijvoorbeeld: Fruitvlieg: we weten dat kenmerk vestigal
aanwezig is op chromosoom 2R.
Nodig? De vermeerderings techniek> PCR
Polymerase Chain Reaction.
Module: PCR analyse en Gelelectroforese
5
PCR MOLGEN2
DNA-isolatie
Voor dat je een organisme wil checken op de aanwezigheid van een
gen, zal je:
•
•
Isolatie houdt in: DNA vrij maken uit een hoeveelheid materiaal.
•
Wij beperken ons tot het onderdompelen van een stukje
bladmateriaal in een bufferoplossing. Die maakt het celmembraan
stuk en bevrijdt het DNA
•
Bij lastige organismen (schimmels ed) moet je soms dik 30 stappen
zetten om het DNA te bevrijden… Lastig,duur en tijdrovend.
•
Gelukkig heeft de biochemische industrie overal ‘kits’ voor op de
markt gebracht die veel werk verlichten.
Als de onderzoeker nog meer analyses moet doen, moet het DNA
zuiver zijn, en vrij van blokkerende stoffen
Module: PCR analyse en Gelelectroforese
6
PCR MOLGEN2
Analysetechnieken
a. DNA-isolatie
b. DNA-amplificatie: PCR
c. Amplicon-detectie: gelectroforese
Module: PCR analyse en Gelelectroforese
7
PCR analyse1
PCR
Wat is PCR?
•
•
Staat voor Polymerase Chain Reaction
Ontwikkeld door de Amerikaan Karry Mullis (1983).
Nobelprijs gekregen.
Wat doet PCR?
•
Gedeelte van het (deels) bekende genoom
vermeerderen (miljarden kopieen)
•
Toepassingen: snelle detectie van ziekteverwekkers,
genen, afwijkende DNAfragmenten etc.
Module: PCR analyse en Gelelectroforese
8
PCR analyse1
We zoeken het rode gen:
..AGCGCGCGCTTTCTCCTCGATCAGTCATCG..
..TCGCGCGCGAAAGAGGAGCTAGTCAGTAGC..
We willen een techniek die alleen het rode gen doet verdubbelen en
niet ál het DNA:
..AGCGCGCGCTTTCTCCTCGATCAGTCATCG..
------------AGTA
CGCT-----------
..TCGCGCGCGAAAGAGGAGCTAGTCAGTAGC..
Leidt tot:
..AGCGCGCGCTTTCTCCTCGATCAGTCATCG..
TCGCGCGCGAAAGAGGAGCTAGTCAGTA
CGCTTTCTCCTCGATCAGTCATCG
..TCGCGCGCGAAAGAGGAGCTAGTCAGTAGC..
Module: PCR analyse en Gelelectroforese
9
PCR analyse1
En dat leidt tot:
..AGCGCGCGCTTTCTCCTCGATCAGTCATCG..
TCGCGCGCGAAAGAGGAGCTAGTCAGTA
CGCTTTCTCCTCGATCAGTCAT
TCGCGCGCGAAAGAGGAGCTAGTCAGTA
CGCTTTCTCCTCGATCAGTCATCG
GCGAAAGAGGAGCTAGTCAGTA
CGCTTTCTCCTCGATCAGTCATCG
..TCGCGCGCGAAAGAGGAGCTAGTCAGTAGC..
Na 40 stappen heb je ca 2^40 van dit soort fragmenten.
Module: PCR analyse en Gelelectroforese
10
PCR analyse1
De Techniek.
Deze methode verlangt een paar
ingredienten:
1. Er is maar heel weinig DNA nodig.
2. Aanwezige primers (stukjes DNA van 20
bp lang).
3. Losse nucleotiden (een mengsel van
dNTP’s)
4. DNA-polymerase (Hittebestendige
versie van het enzym dat nucleotiden
aan het enkele DNA vasthecht)
5. Omgevingsfactoren (MgCl2) , Water ed.
Module: PCR analyse en Gelelectroforese
11
PCR analyse1
Hoe werkt het principe?
• Bij hoge temperatuur smelten de DNA
strengen en raken uiteen (98 graden C)
• Dan hechten zich korte apart vervaardigde
stukjes enkelstrengs DNA (zgn primers) (bij
een bepaalde temp.
• Hierna koppelt DNApol er losse nucleotiden
aan, en maakt de nieuwe strengen af.
• Deze drie stappen herhaal je 30-40x.
• Tenslotte koelt het geheel weer af,en heb
je enorme hoeveelheid van gekopieerd
fragment DNA.
Module: PCR analyse en Gelelectroforese
12
PCR analyse1
1a gewone dubbelstrengs DNA
1b DNA Smelt bij 98 graden
1c bij ca 50 graden hechten
primers
1d bij 72 graden worden deze
aangevuld met losse nucleotiden
door enzym Taq-DNApolymerase
(Taq -= Thermo aquatic)
2b Opnieuw smelt bij 98 graden
Module: PCR analyse en Gelelectroforese
13
PCR analyse1
2c bij ca 50 graden hechten
primers
2d Polymerase knoopt er opnieuw
losse nucleotiden aan en verlengt
de streng tot het einde. (Bij 72
graden)
3b Opnieuw smelt bij 98 graden
voor ronde 3….
Etc etc etc..
Module: PCR analyse en Gelelectroforese
14
PCR analyse1
Wat valt op?
• Elke ronde verdubbelt het
aantal korte fragmenten.
Dus na 40 rondes heb je in
principe 240 fragmenten.
• Het aantal grote strengen
blijft gelijk
• Het aantal ‘halve’ strengen
neemt elke stap lineair toe.
• Na 40 ronden is het aantal
korte fragmenten dermate
talrijk dat zij voor het blote
oog kunnen worden
aangetoond.
(Gel-electroforese).
Module: PCR analyse en Gelelectroforese
15
PCR analyse1
Wat is de werkwijze in de praktijk?
A)
We moeten DNA zien te halen uit de cellen van het
organisme dat we onderzoeken. (plant)
B)
C)
Hiervan is maar heel weinig DNA nodig
We voegen de ingredienten voor replicatie toe:
water
DNA-nucleotiden
primers
Taq-DNA-polymerase (enzym)
zouten ed.
D)
Dit mengsel doorloopt een herhaald traject van
temperaturen (98 graden, 50 graden, 72 graden).
E)
Tenslotte is het mengsel verrijkt met korte
fragmentjes.
(Zó talrijk dat de rest nauwelijks meetelt..)
Module: PCR analyse en Gelelectroforese
16
PCR analyse1
1.
Epje 0.2 ml met
verdunningsbuffer
2. Voeg 2 mm2 blad
toe
3. Crush met
pipetpunt
4. Centrifugeer
5. Neem supernatant
over in schoon epje
6. Voeg toe:
• Primers
• dNTP’s, Mgcl2
mengsel
• DNA polymerase
• Water
En dan….IN DE PCR!
Module: PCR analyse en Gelelectroforese
17
PCR analyse1
PCR: Techne CYCLOGENE
1.
2.
Verwarmd deksel
3.
Aparte instructie
aanwezig.
4.
Bedieningspaneel
Ruimte voor de
epjes (0.2 ml)
96 stuks maximaal
1. Ruimte voor 96 epjes
2. Verwarmd deksel voorkomt
verdamping.
Module: PCR analyse en Gelelectroforese
18
PCR analyse1
Zorg dat je alles bij
de hand hebt.
1. Centrifuge
2. Pipetten
3. Puntjes
4. Rekje voor epjes
5. Chemicalien
6. Handschoenen
7. Stift
8. Afvalvat
9. Tissues
10. Vortex/shaker
Dit type practicum EIST dat je je volledig voorbereid.
Module: PCR analyse en Gelelectroforese
19
PCR analyse1- deel
GELELECTROFORESE
Electroforese
• DNAfragmenten zijn negatief geladen en
zullen in een electrisch veld van MIN naar
PLUS bewegen.
• De grootte van de fragmenten bepalen de
migratiesnelheid. Grote langzaam, kleine
snel!
• Methode: Men maakt een gel van agarose
(soort zeewierextract)
• Hierin worden kuiltjes/welletjes aangebracht.
• De hele gel gaat in een buffer, waarmee ook
de gel gemaakt is.
• Na 1-2 uur ‘runnen’ zullen de diverse DNA
fragmenten zich scheiden op basis van hun
grootte.
Module: PCR analyse en Gelelectroforese
20
PCR analyse1- deel
GELELECTROFORESE
Module: PCR analyse en Gelelectroforese
21
Het ‘home-made’
electroforese-bakje.
• De gel ligt verhoogd
• Links en rechts
aansluitingen
• Ernaast ligt het
kammetje dat wordt
gebruikt om tijdens het
stollen van de gel de
kuiltjes (welletjes) te
maken.
• In één welletje past ca
30 uL.
• Hiernaast de bak
aangesloten op 100
volt.
• Deze gel is bijna
halverwege: de kleuren
verraden hoevér je
bent.
PCR analyse1- deel
GELELECTROFORESE
• Deze gel is bijna
halverwege: de kleuren
verraden hoevér je
bent.
• Agar is niet geschikt.
Te grof en de zaak
wordt diffuus.
Module: PCR analyse en Gelelectroforese
22
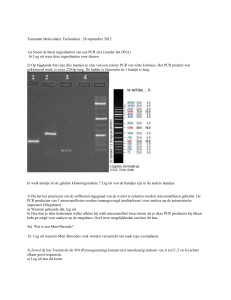
PCR analyse1- deel GELELECTROFORESE: het resultaat
Welletjes
Ruler
bandje
Let op: de ruler 50bp, de helderheid van bandjes.
Module: PCR analyse en Gelelectroforese
23
PCR analyse1
Werkwijze in detail.
Het hele proces laat zich verdelen in drie etappes.
1. DNA-isolatie uit moedermateriaal.
Voor dit practicum zijn dat bladeren van de
aardappel
2. DNA-PCR techniek voor amplicons
3.
Gel-electroforese
Module: PCR analyse en Gelelectroforese
24
PCR analyse1
Werkwijze in detail. DNA-ISOLATIE
•
Het zuiver in handen krijgen van DNA is een
lastige klus die veelal ingewikkelde chemicalien
en handelingen vergt.
• Er zijn ‘kits’ op de markt die dat proces a.h.w.
met een kookboekrecept kunnen maken. Die
werken prima maar zijn erg duur (vanaf 300400 euro voor 50 reacties..)
• Wij gebruiken de Phire-Plant PCR kit waarmee
eenvoudige plantaardige samples kunnen
worden behandeld. Nadeel: er komen veel
vervuilingen mee en verdere analyse van het
DNA kan dus niet.
Module: PCR analyse en Gelelectroforese
25
PCR analyse1
Werkwijze in detail. DNA-ISOLATIE- 2
1.
In een klein epje van 0.2 ml wordt 10 uL buffer
gedaan.
2.
Men snijdt op een objectglaasje met schone scalpel
een stukje blad/stengel af ter grootte van 1 x 2
mm.
3.
4.
Dit wordt erbij gegooid.
5.
6.
1 minuut centrifuge 10000-15000 rpm
Met een plastic pipetpunt wordt het materiaal
‘gecrusht.’. Het ziet nu groen van de chlorophyll.
Overpipetteren van het schone supernatant in een
schone ep van 0,2 ml.
Wat gebeurt er?
Het DNA dat aan randen zit van het stukje blad is vrij
gekomen en wordt door de centrifuge niet naar
beneden gedrukt. De bladresten wel. De buffer
lyseert enigszins ook de cellen, zodat er meer DNA
kan vrijkomen.
26
Module: PCR analyse en Gelelectroforese
PCR analyse1
Werkwijze in detail. PCR 1
1. Van het supernatant wordt maar 0,5 uL monster
genomen. (dat is érg weinig… maar genoeg!)
2. Hierbij worden in volgorde toegevoegd:
3. 0,4 uL primer A
4. 0.4 uL primer B
5. 10 ul PCR buffer (bevattende de dNTP’s, MgCl2
etc)
6. 0.4 uL Taq-Polymerase.
7. Aanvullen tot 20 uL vloeistof met water dat geen
dNase bevat (aquadest dat even gekookt heeft).
Men heeft de concentraties zó gekozen dat de
hoeveelheden passenbij de reacties. Elk epje bevat
zo steeds 20 uL reactiemengsel.
Module: PCR analyse en Gelelectroforese
27
PCR analyse1
Werkwijze in detail. PCR 2
Vervolgens:
1. Instellen PCR apparaat op programma 20
2. Dit impliceert:
• 1e ronde 10 min 98 graden
• 2e ronde 10 sec 98 graden, 10 sec 52 graden, 30
sec 72 graden.
•
•
Stap twee nog 39 x herhalen.
3e ronde: 5 minuten op 72 graden.
Laden epjes. PCRapparaat aan, heated lid ook
aan, goeie programma selecteren en GO!
Module: PCR analyse en Gelelectroforese
28
PCR analyse1
Werkwijze in detail. PCR 3
Vervolgens:
1. Instellen PCR apparaat op programma 20
2. Dit impliceert:
• 1e ronde 10 min 98 graden
• 2e ronde 10 sec 98 graden, 10 sec 52 graden, 30
sec 72 graden.
•
•
Stap twee nog 39 x herhalen.
3e ronde: 5 minuten op 72 graden.
Laden epjes. PCRapparaat aan, heated lid ook
aan, goeie programma selecteren en GO!
Module: PCR analyse en Gelelectroforese
29
PCR analyse1
Werkwijze in detail. Maken van de gel.
1.
2.
3.
4.
5.
Neem 25 ml 10 xTBE-buffer.
Voeg 225 ml aquadest toe. (10 verdund).
Neem hiervan 80 ml.
Voeg 1,6 gram agarosepoeder.
Verhit in d magnetron voor 45 sec en
zwenk
6. Verhit verder totdat het bijna kookt en
de agarose is gesmolten en helder is.
7. Laat afkoelen tot ca 60 graden
8. Pipetteer 6 uL EthidiumBromide (giftig en
carcinogeen!) erbij.
9. Giet dit in het bakje nadat je de
scheidingswandjes geplaatst hebt.
10. Plaats het 9 holes kammetje bij de minpool.
11. Cool down…. Min 30-60 min.
Module: PCR analyse en Gelelectroforese
30
PCR analyse1
Module: PCR analyse en Gelelectroforese
Werkwijze in detail. Laden van de GEL
1. Voeg aan elk PCR-epje 6 ul loading dye
Dit maakt het inladen zichtbaar.
2. Haal, als de gel goed gestold is, het
kammetje eruit.
3. Vul de gelchamber met TBEbuffer in
dezelfde concentratie als waarmee de
gel is gemaakt.
4. Vul elke welletje met 20 ul mengsel
vanuit de epjes met monster én
loadingdye.
5. Sluit de chamber met de deksel
6. Sluit de voeding aan op 50 Volt en zet de
zaak aan voor 10 min.
7. Na 10 min over op 100 Volt.
8. Na afloop eerst de spanning eraf.
9. Chamber leeggieten in opvangbak.
Kijk uit dat de gel er niet uitvalt.
31
PCR analyse1
Werkwijze in detail. Bekijken van de gel met
UV.
Het EtBr hecht zich aan DNA en is
fluoriserend als het met UV wordt
beschenen.
Kijk NOOIT in de UV lamp
Als het goed is, is de DNA ladder 50 bp te
zien als een reeks bandjes.
1000, 900, 800, 700, 600, 500, 400, 300, 250,
200,150, 100, 50 basepairs.
1. Maak een digitale foto
2. Zet de lamp snel uit.
3. Verpak de Gel in plastig, label en mik het
in de vriezer. Daardoor verlopen de
bandjes niet en kan je later de zaak nog
na eens bekijken.
Module: PCR analyse en Gelelectroforese
32
PCR analyse1
Module: PCR analyse en Gelelectroforese
Werkwijze in detail. Bekijken van de gel
met UV.
SOMS gaat het gewoon MIS…..
33
PCR analyse1
Module: PCR analyse en Gelelectroforese
Werkwijze in detail. Bekijken van de gel
met UV.
SOMS gaat het gewoon GOED!
34
PCR analyse1
Hierna volgt de module:
DNALAB1 Solanum
Of
DNALAB2 DROS
Of
DNALAB3 CSI
In alle gevallen: Lees en bestudeer je
handleiding!!
En werk aandachtig. Deze spullen zijn
kostbaar!!
Module: PCR analyse en Gelelectroforese
35
PCR analyse1
Verder nog:
Sequencing:
http://www.youtube.com/watch?v=8n2LvJ-m0n0
MIT: college over DNA-technieken:
http://www.youtube.com/watch?v=uDXH6Uu0ghc
http://www.youtube.com/watch?v=PRy4rRdDbk&list=PLF83B8D8C87426E44
http://www.youtube.com/watch?v=QTb6YsxMbBY
Module: PCR analyse en Gelelectroforese
36