16
door Mark Mieras
Nieuwe paarden voor de
ziekte van Alzheimer
De strijd tegen de ziekte van Alzheimer vergt een lange adem. Akademie
Nieuws publiceerde meerdere keren over veelbelovende ontwikkelingen
die de genezing volgens onderzoekers dichterbij of zelfs onder handbereik
brachten. Waar blijft het wondermiddel toch?
Neurowetenschapper Fred van Leeuwen haalde in 1998
de omslag van Science met zijn ontdekking dat Alzheimer samenhangt met een afleesfout van de genetische
code ‘GAGAG’: er valt een ‘GA’ weg. De ontdekking was
een belangrijk moment in zijn wetenschappelijke loopbaan, herinnert hij zich. ‘In één maand gaf ik dertig interviews, onder andere aan de BBC, en het haalde ook de
Times.’
domper
De ontdekking gaf richting aan Van Leeuwens onderzoek
in de daaropvolgende jaren. Eerst aan het Nederlands Instituut voor Neurowetenschappen (NIN-KNAW) in Amsterdam en sinds 2007 aan de Universiteit Maastricht.
‘Onze ontdekking is meerdere malen door buitenlandse
onderzoeksgroepen bevestigd en uitgebreid. Zelf hebben
we recent, in een transgene muizenlijn, aangetoond dat
een genetische afleesfout van het ubiquitine-gen inderdaad tot Alzheimerachtige verschijnselen leidt: je ziet bij
Gesneuveld lijkt ook
het ‘Alzheimer-vaccin’
de muizen een significante vermindering van de synaptische plasticiteit en hun ruimtelijk geheugen.’
De afleesfout wordt volgens Van Leeuwen zichtbaar
bij ouderdom. ‘We hebben een biomarker ontwikkeld om
het te kunnen meten. De fout ontstaat geleidelijk vanaf
een jaar of vijfenvijftig, en kan bijdragen aan andere neurodegeneratieve ziekten, zoals die van Huntington.’
Of je Alzheimer krijgt, hangt volgens Van Leeuwen
af van de combinatie met andere factoren. De leesfout
kan het eiwit ubiquitine treffen, dat bij hersencellen een
belangrijk rol speelt voor de afbraak van afwijkende eiwitten. Van Leeuwen: ‘Dat beïnvloedt de vorming van de
plaques: de afzettingen van β-amyloïd buiten de hersencellen, die je na de dood in de hersenen van Alzheimerpatiënten aantreft.’
In juli vormde dit bericht een zware domper op de
jaarlijkse bijeenkomst van de Alzheimer Association in
Chicago. Gesneuveld lijkt ook het ‘Alzheimer-vaccin’ dat
het Britse farmaceutische concern Elan in ontwikkeling
had. Het vaccin mobiliseert het afweersysteem om de
plaque als een lichaamsvreemde stof af te breken.
overleven
Het wereldwijde onderzoek naar de ziekte van Alzheimer
lijkt op het verkeerde paard te hebben gewed. De adepten van de plaques-hypothese houden nu nog vast aan de
veronderstelling dat mensen bij wie Alzheimer is vastgesteld al te ver heen zijn om nog baat te hebben bij verwijdering van de plaques. Nieuwe biomarkers voor de diagnostiek zullen volgens hen uitkomst bieden. Daarmee
kan de ziekte in een eerder stadium worden vastgesteld,
zodat je eerder met medicatie kunt beginnen. Maar Van
Leeuwen gelooft er niet in. ‘Ik kan mij niet voorstellen
dat mensen met een beginnende Alzheimer kiezen om
zich te laten behandelen. De kans is groot dat de plaques
uiteindelijk niet de oorzaak maar een symptoom van de
ziekte blijken te zijn. Mogelijk ontstaat de echte schade
door het tau-eiwit dat zich binnen de hersencellen afzet.
Bij recente medicijn-trials bleek het verdwijnen van de
plaques bij patiënten geen verbetering op te leveren in
hun functioneren.’
Akademie Nieuws december 2008
17
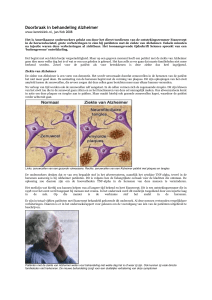
Overlevende neuronen (pijlen) in menselijk
postmortem hersenweefsel zonder (A) en met
hulp van neurale stamcellen (B)
Er is dus grote behoefte aan een nieuwe benadering
van de ziekte van Alzheimer. Ook onderzoeker Ronald
Verwer van het NIN anticipeert daar al jaren op. Verwer
slaagde er als eerste in om menselijke hersencellen
buiten het lichaam tientallen dagen in leven te houden in
dunne coupes. Van de Nederlandse Hersenbank, die zeer
snelle hersen-obducties van overleden patiënten verzorgt,
Hersencellen vertonen meer levenskracht
in de nabijheid van stamcellen
krijgt hij hersenweefsel. Verwer toonde onder andere aan
dat zwaar door Alzheimer aangetaste hersencellen toch
lang kunnen overleven. ‘De cellen worden wel kleiner
maar ze gaan niet snel dood.’ Het celverlies dat we lang
met Alzheimer associeerden berust volgens Verwer
vooral op telfouten.
dopaminekraan
‘Onze aanpak geeft aan dat wij anders denken’, zegt Verwer: ‘Mijn hypothese is dat de extracellulaire afzetting van
β-amyloïd en de afzetting binnen de cellen van tau het
gevolg zijn van de dalende celactiviteit. Niet omgekeerd!
Voor iemand Alzheimer krijgt, zie je een fase waarin de
hersenen al een verminderd metabolisme vertonen, terwijl er verder nog geen pathologische afwijkingen zijn. Je
ziet de cognitieve functies langzaam achteruit gaan. Deze
mensen worden mild cognitively impaired genoemd. Die
daling van het metabolisme lijkt samen te hangen met
degeneratie van cellen in de ‘nucleus basalis van Meynert’,
een hersencentrum met uitlopers door de hele hersenschors.’
Het lijkt er dus op dat de hersenen hun eigen thermostaat omlaag draaien geruime tijd voor de eiwitafzettingen
ontstaan. Verwer: ‘Je ziet bij Parkinson een vergelijkbaar
proces. Daar zijn het de degenererende cellen in de substantia nigra, de zwarte stof, die het proces inzetten door
de dopaminekraan naar de basale ganglia dicht te draaien.
De basale ganglia is belangrijk voor het reguleren van
bewegingen. De redenen van deze degeneratieve processen kennen we niet, wel weten we dat veroudering een
belangrijke risicofactor is. En veroudering is nog altijd een
ongrijpbaar proces.’
niet verwonderlijk
Verwer zoekt naar mogelijkheden om de aangetaste cellen te revitaliseren, in de hoop het proces te stoppen
of zelfs te keren. Dankzij de coupes met nog levende
hersencellen kan hij methoden uittesten. Succesvol was
tot nu toe de blootstelling aan stamcellen. Daarvan is bekend dat ze andere cellen in hun omgeving gezonder en
actiever maken. Ook hersencellen vertonen in de nabijheid van stamcellen meer levenskracht. Onbekend is nog
welk van de stoffen die de stamcel uitscheidt, voor dit
effect zorgt. Het is er overigens niet alleen voor Alzheimer. Ook cellen van niet-Alzheimer-patiënten reageren
positief op de aanwezigheid van de stamcellen. Verwer:
‘Maar dat is misschien niet verwonderlijk. Door het ingewikkelde proces van het uitnemen van het hersenweefsel, het transport vanuit de obductieruimte naar het NIN
en de kweek, verkeren ook gezonde hersencellen in een
minder goede conditie.’