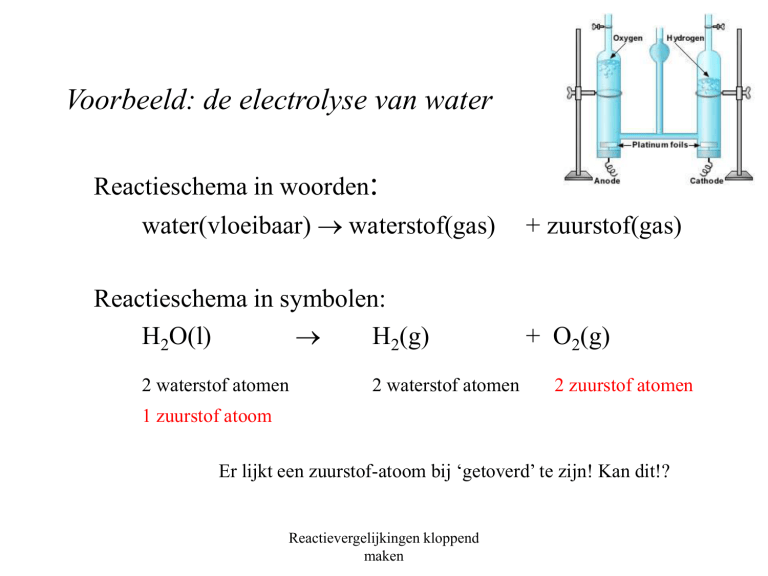
Voorbeeld: de electrolyse van water
Reactieschema in woorden:
water(vloeibaar) waterstof(gas)
Reactieschema in symbolen:
H2O(l)
H2(g)
2 waterstof atomen
2 waterstof atomen
+ zuurstof(gas)
+ O2(g)
2 zuurstof atomen
1 zuurstof atoom
Er lijkt een zuurstof-atoom bij ‘getoverd’ te zijn! Kan dit!?
Reactievergelijkingen kloppend
maken
H2O(l)
H2(g)
Reactievergelijkingen kloppend
maken
+
O2(g)
2H2O(l)
2 moleculen water
4 waterstof atomen
2 zuurstof atomen
2 moleculen waterstof
4 waterstof atomen
2H2(g)
+
O2(g)
1 molecuul zuurstof
2 zuurstof atomen
N.B. De ‘één’ (zoals voor O2 in ons voorbeeld) wordt niet vermeld
Reactievergelijkingen kloppend
maken
Neem de volgende reactievergelijkingen over
en maak ze kloppend:
a. …H2 (g) + …Cl2 (g) …HCl (g)
b. ...Mg (s) + ...O2(g)
...MgO
c. …Fe (s) + …O2(g)
Fe2O3 (l)
d. …FeS(s) + …O2(g)
…SO2(g) + …Fe2O3(s)
Reactievergelijkingen kloppend
maken
Neem de volgende reactievergelijkingen over en
maak ze kloppend:
a. …CO2(g)
+ …Mg(s)
…C(s) + …MgO(s)
b. ...H2O(l)
+ ...F2(g)
...HF(aq) + ...O2(g)
c. …NH3(g)
+ …O2(g)
…NO(g) + …H2O(l)
d. …FeS(s)
+ …O2(g)
…SO2(g) + …Fe2O3(s)
Reactievergelijkingen kloppend
maken
Tips:
• Gebruik zonodig breuken om de rv kloppend te maken.
Vermenigvuldig dan dusdanig dat er gehele getallen in de
rv staan.
C5H5(l)
+ 6¼O2(g)
5CO2(g) + 2½ H2O(l)
4C5H5(l) + 25O2(g)
20CO2(g) + 10H2O(l)
• Bewaar moleculen die uit één atoomsoort bestaan voor het
laatst. Hier kun je namelijk alle getallen voor zetten,
zonder dat het invloed heeft op andere atoomsoorten.
• Gebruik zo laag mogelijke gehele getallen, dus niet
8C5H5(l)
+ 50O2(g)
40CO2(g) +
20H2O(l)
• Extra oefeningen:
Reactievergelijkingen kloppend
maken
http://www.ping.be/ursula/chemoef/reactievgl.htm












