Hoofdstuk 1
Basic cardiac structure and function
-
-
-
-
-
-
-
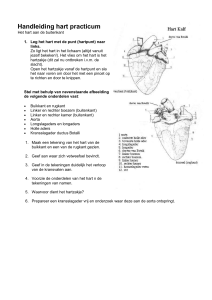
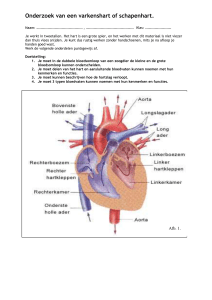
Pericardium: zak om het hart
o Fibreuze buitenste laag (parietaal pericard)
o Dunne pericardvocht film
o Sereuze binnenste laag (visceraal pericard)
Oppervlaktes van het hart:
o Apex: top van linker ventrikel
o Basis of posterieur oppervlak: rechter en vooral linker atrium, tussen de longhili
o Anterieur oppervlak: rechter atrium en ventrikel
o Inferieur oppervlak: rechter en vooral linker ventrikel, langs het diafragma
Kleppen
o Atrioventriculair
Links: mitralisklep
Rechts: tricuspidalisklep
o Semilunair
Aortaklep
Pulmonaalklep
Endocardium: enkele laag endotheelcellen aan de binnenzijde van de hartkamers en over de
hartkleppen
Subendocardiaal weefsel: fibroblasten, elastische en collageenvezels, venen, zenuwen en
takken van het geleidend systeem
Myocardium: dikste laag bestaande uit cardiale spiercellen
Extern van het myocard een bindweefsellaag met vetweefsel en grotere bloedvaatjes
Epicardium = visceraal pericard
Rechter atrium:
o Vena cava inf. en sup. en de sinus coronarius komen hierin uit
o Tricuspidalisklep naar ventrikel
Rechter ventrikel
o Kegelvormig outflow traject richting a. pulmonaris met gladde wand
o Overige wanden sponsachtig door trabeculae carnae
o Moderator band: grote trabekel die een component van de rechter bundel tak draagt
o Drie papillairspiertjes die via chordae tendinae verbonden zijn aan de klepbladen van
de tricuspidalisklep
o Pulmonaalklep naar a. pulmonalis
Linker atrium:
o Vier pulmonaalvenen komen hierin uit
o Mitralisklep naar ventrikel
Linker ventrikel
o Vestibulum aortae is het gladde outflow traject richting aorta
o Overige wanden bedekt met meer en fijnere trabeculae carnae dan rechter ventrikel
o Wee papillairspiertjes met minder en dikkere chordae tendinae dan rechts,
verbonden aan de klepbladen van de mitralisklep
o Aortaklep naar aorta met coronaire aftakkingen direct distaal van de klepbladen
1
-
-
-
-
-
Intraventriculair septum
o Klein membraneus deel juist onder de aortaklep
o Groot musculair deel dat door de hogere hydrostatische druk in het linker ventrikel,
uitpuilt in het rechterventrikel
Impulse geleidend systeem
o SA knoop (sinoatriaal) in de wand van het rechter atrium
o AV knoop (atrioventriculair) in het inferoposterieur deel van het interatriaal septum
o Bundel van His doorheen interventriculair septum
o Bifurcatie van bundel in een linker bundel tak (brede waaier van vezels) en een
rechter bundel tak (compacte bundel)
o De vezels eindigen als Purkinje vezels die de impuls gaan geven aan de ventriculaire
spiercellen (als eerst de papillairespiertjes, zodat deze eerder contraheren dan de
rest van het ventrikel en er geen regurgitatie plaatsvindt)
Coronaire arteriën
o Linker hoofdtak loopt tussen linker atrium en t. pulmonalis naar anterieur
LAD (left ascending artery) volgt de anterieure interventriculaire groeve en
bevloeit het anterieure tweederde van het interventriculair septum en de
anterieure wand van het linker ventrikel
CXA (circumflex artery) loopt door de atrioventriculaire groeve naar
posterieur en bevloeit de laterale en posterieure wand van het linker
ventrikel
o Rechter hoofdtak (RCA) loopt door de rechter atrioventriculaire groeve
Marginale takken bevloeien de anterieure en laterale wand van het rechter
ventrikel
AV knoop arterie
PDA (posterior descending artery) bevloeit de inferieure en posterieure
wand van beide ventrikels en het posterieure éénderde van het
interventriculair septum
Deze situatie noemen we rechtsdominant en komt voor bij 85% van
de bevolking. De PDA kan echter ook van de CXA komen
(linksdominant) of de bevloeiing van de posterieure zijde van het
hart gebeurt door takken van zowel CXA als RCA (codominant).
o SA knoop arterie kan komen van RCA (70%), CXA (25%) of beide (5%)
o Spiervezels die zich juist subendocardiaal bevinden worden bevloeit door de
coronaire ofwel door de thebesische venen, kleine vasculaire kanaaltje direct vanuit
de ventriculaire caviteit
Coronaire venen volgen ongeveer dezelfde routes als de arteriën (superficiëel daarvan) en
draineren in de sinus coronarius in het rechter atrium. Ook de thebesische venen verzorgen
een klein deel van de veneuze retour
Myocyten
o Streping gelijk skelet spiercellen
o Één of twee nucleï
o Myocyt > myofibril > sarcomeer
o Celmembraan = sarcolemma
o Intercalaire schijven: gap junction complexen tussen opeenvolgende vezels
2
o
-
-
-
T-tubules: invaginaties in het sarcolemma, vergroten contactoppervlak met
extracellulaire omgeving zodat ionentransport en daarmee geassocieerde excitatie
en relaxatie sneller kan gebeuren
o Sarcoplasmatisch reticulum is complementair met de t-tubules en bevat de
intracellulaire calciumvoorraad
Exciteerbare cellen in het hart:
o Ventriculaire en atriale spiercellen
Fase 4: rustpotentiaal -90 mV (kaliumkanalen open)
Fase 0: snelle depolarisatie (vanuit naburige cel via gap junction) openen
van de snelle natrium kanalen, positieve feedback loop
Threshold voor actiepotentiaal -70 mV, snelle inactivatie van de
snele natrium kanalen
Fase 1: snelle repolarisatie tot 0 mV door transiënt geactiveerde kalium
kanalen
Fase 2: plateaufase door outflow van kalium en inflow van calcium door Ltype calium kanalen (openen al tijdens fase 0 op -40 mV)
Inflow van calcium triggert interne calcium release uit SR voor
contractie van myocardcellen
Fase 3: calcium kanalen sluiten, repolarisatie door kalium outflow tot -90 mV
o Gespecialiseerd snel geleidend weefsel (purkinjevezels)
Gelijk de ventriculaire en atriale spiercellen, met iets negatievere
rustpotentiaal en iets snellere fase 0 upstroke
o Pacemakercellen (SA-knoop, AV-knoop)
Fase 4: maximaal negatief voltage van -60 mV, spontane depolarisatie door
pacemaker current (voornamelijk natrium) tot threshold op -40 mV
Snelle natriumkanalen in inactieve staat
Fase 0: depolarisatie door inflow van relatief trage calcium kanalen
Lagere aplitudo dan ventriculaire en atriale spiercellen
Calcium kanalen sluiten, repolarisatie door kalium outflow tot -60 mV
Refractoire periode
o Absoluut: tijdens fase 0, 1 en 2, alle snelle natrium kanalen zijn dicht en er is geen
actiepotentiaal mogelijk
o Effectief: iets doorlopend in fase 3, wanneer enkele natriumkanalen geopend zijn en
een gelokaliseerde actiepotentiaal mogelijk is maar geen propagatie
o Relatief: de rest van fase 3, hierin kan een actiepotentiaal doorgeleid worden maar
langzamer en zwakker dan normaal
AV-knoop: de enige elektrische verbinding tussen de atria en ventrikels, hier treedt
vertraging op zodat de atria zich volledig kunnen legen voordat de ventrikels samentrekken.
Het functioneert ook als gatekeeper wanneer er abnormaal snelle atriale contracties zijn.
3
Hoofdstuk 2
The cardiac cycle: mechanisms of heart
sounds and murmurs
-
-
-
Ventriculaire drukken:
o Systole: ventriculaire contractie, begint met sluiten van de mitralis- / tricuspidalisklep
(S1)
o Diastole: ventriculaire vulling, begint met sluiten van de aorta- / pulmonaalklep (S2)
Atriale drukken:
o A-wave: atriale contractie (geeft ook drukstijging in ventrikels)
o C-wave: mitralis- / tricuspidaliskleppen sluiten en bulken uit in atria
o V-wave: passieve vulling van de atria vanuit systemische en pulmonaal venen
Jugulair veneuze pols: representatief voor de rechter atrium druk
Hartgeluiden
o S1: sluiten van de mitralis- / tricuspidalisklep
Duidelijkst te horen t.h.v. apex (5e i.c. li) met diafragma (hoog frequent)
Niet hoorbaar gesplitst
Luidheid afhankelijk van de afstand tussen de open klepbladen, de
beweeglijkheid van de klepbladen en snelheid van ventriculaire drukstijging
(luider bij verkorte duur van de diastole)
o S2: sluiten van de aorta- / pulmonalisklep
Variabel met ademhaling: fysiologische hoorbare splitsing tijdens inspiratie.
Abnormale splitsing:
Verwijde splitsing: groter interval tussen het sluiten van de aortaklep
en van de pulmonalisklep, zelfs tijdens expiratie is S2 gesplitst: te laat
sluiten van de pulmonalisklep (rechter bundel tak blok)
Gefixeerde splitsing: S2 is gesplitst met onveranderd interval tijdens
zowel inspiratie als expiratie (atriaal septum defect)
Paradoxale splitsing: S2 is gesplitst tijdens expiratie maar niet tijdens
inspiratie: te laat sluiten van de aortaklep (linker bundel tak blok,
aortastenose)
Duidelijkst te horen t.h.v. 2e i.c. li parasternaal met diafragma (hoog
frequent)
4
-
Luidheid afhankelijk van de snelheid van het bloed dat terugstroomt in de
arteriën richting ventrikels na systole en hoe plots deze beweging word
gestopt door het sluiten van de kleppen
o Extra systolische geluiden
Ejectieklik
vroeg systolisch
openen van de aorta- / pulmonalisklep
2e i.c. li parasternaal, diafragma
Aorta- / pulmonalisklepstenose of dilatatie van de aorta / a.
pulmonalis
Onderscheid aorta/pulmonaal: aorta ook te horen aan de apex,
pulmonaal enkel aan de basis te horen en heeft een verminderde
intensteit bij inspiratie
Mid- of laat systolische geluiden (veroorzaakt door mitralis- / tricuspidalis)
o Extra diastolische geluiden
Opening snap
Openen van de mitralis- / tricuspidalis klep
Mitralis- /tricuspidalisklepstenose
Apex, diafragma
Verwarring met splitsing van S2: tijdens inspiratie worden bij opening
snap 3 geluiden achter elkaar gehoord en bij expiratie 2
Hoe ernstiger de stenose, hoer korter het interval tussen S2 en OS
S3
Vroeg diastolisch
Expansie van de chordae tendinae tijdens ventriculaire vulling
Apex in linker decubitus houding, klok
Normaal in kinderen en jongvolwassenen
Ook wel: ventriculair gallop
S4
Laat diastolisch
Contractie van de atria tegen stijf ventrikel (hypertrofie, ischemie)
Apex in linker decubitus houding, klok
Ook wel: atriaal gallop
Summatie gallop
Patiënt met zowel S3 als S4 met daarbij tachycardie, zodat de 2 tonen
samensmelten
Pericardiale knock
Constrictieve pericarditis
Zeer moeilijk te onderscheiden van OS of S3
Geruisen worden veroorzaakt door
o Pariële obstructie (stenoses)
o Verhoogde flow
o Ejectie in een gedilateerde kamer
o Regurgitatie
5
-
-
-
-
o Abnormale shunting (bijv. Ventriculair septum defect)
Beschrijving van een geruis:
o Intensiteit
VI stadia voor systolisch
IV stadia voor diastolisch
o Frequentie
Hoog
Laag
o Vorm
Diamand
Crescendo ...
o Locatie
Aorta: 2e i.c. re parasternaal
Pulmonalis: 2e i.c. li parasternaal
Tricuspidalis: linker onderboord sternum
Mitralis: apex, 5e i.c. li
o Radiatie
Systolische geruisen
o Ejectiegeruis
Aorta- / pulmonalisklepstenose
Diamandvormig
Vaak in combinatie met ejectie klik
Radiatie naar nek mogelijk
o Pansystolisch geruis
Mitralis- / tricuspidalisklepregurgitatie of ventriculair septum defect
Uniform
Radiatie naar axilla mogelijk (niet bij VSD)
o Laat systolisch geruis
Mitralisklepregurgitatie door mitralisklep prolaps in het linker atrium
Vaak in combinatie met een mid-systolische klik
Diastolische geruisen
o Vroeg diastolisch geruis
Aorta- / pulmonalisklepregurgitatie
Decrescendo
o Mid- tot laat diastolisch geruis
Mitralis- / tricuspidalisklepstenose of abnormaal verhoogde flow
Vaak in combinatie met opening snap
Decrescendo tot verdwijnen, met terug crescendo tegen eind diastole
Continuë geruisen
o Openstaande ductus arteriosus (PDA): diamandvomig
o Aorta- / pulmonalisklepstenose EN –regurgitatie: to-and-fro, gescheiden diastolische
en systolische component
6
Hoofdstuk 3
Cardiac imaging and catheterization
-
Röntgen thorax
o Postero-anterieure opname
Linker ventrikel grootte
linker atriaal aanhangsel
a. pulmonalis
aortaboog
v. cava superior
o Laterale opname van rechts naar links
Rechter ventrikel grootte
Posterieure boorden van linker atrium en ventrikel
Anteroposterieure thorax diameter
o Hartschaduw
Cardiothoracale ratio normaal kleiner dan 0.5
Corrigeren bij hoogstand van het diafragma of verminderde
anteroposterieure diameter van de thorax
Vergroot hart onderscheiden van periardiale effusie
Hypertrofie zonder dilatatie kan onopgemerkt blijven, omdat de hypertrofie
meestal ten koste gaat van het interne volume van de kamer
Dilatatie van de kamers wijst op (niet accuut)
Hartfalen
Kleplijden
Shunts
Pulmonaire afwijkingen
Dilatatie van de aorta wijst op
Aneurysma
Dissectie
Aortaklepinsufficientie
Atherosclerose
Dilatatie van de a. pulmonalis wijst op
Left-to-right shunts
Pulmonaire hypertensie door andere oorzaken
o Pulmonale bevindingen
Verhoogde pulmonaire veneuze druk
Redistributie van bloed van de bases naar de apices van de longen
Pulmonaire oedeem
o Vanuit hilaire regio, ‘vlinder patroon’
o Kerley B lijntjes: horizontale lijntjes in de preiferie van de
long ter hoogte van de basis die wijzen op vocht in
interlobulaire ruimtes
Pleurale effusie
o Vervagen van de costodiafragmatische sinussen
7
-
Echocardiografie
o Transthoracaal
o Transoesofagaal
Aorta of atriale imaging
Atriaal aanhangsel
Transthoracaal geeft onvoldoende goed beeld (bijv. COPD)
Prostetische kleppen
o M-mode: accurate meting wanddikte en klepbeweging
o 2D: anatomische verhoudingen en de beweging van cardiale structuren in relatie tot
elkaar, wanden, klepbeweging en massa’s
o Doppler: bloed flow richting en snelheid, turbulenties, drukgradiënten
-
𝑓𝑠 × 𝑐
𝑣 = 2𝑓0 (𝑐𝑜𝑠𝜃)
v = snelheid m/sec
fs = doppler frequency shift kHz
c = snelheid van geluid in lichaamsweefsel m/sec
f0= frequentie van geluid uit de transducer MHz
θ = hoek tussen uitgezonden geluid pulse en de as van de bloedflow
o Ventriculaire assesment
Wanddikte, massa en ejectiefractie
Diastolische functie
o Kleplijden
Drukgradiënt over gestenotiseerde klep
o Coronary artery disease
Abnormaliteiten die consequentie zijn van ischemisch myocard
Stress echocardiografie: induceerbaar myocardiale ischemie aantonen
o Cardiomyopathie
Onderscheid tussen gedilateerde, hypertrofische en restrictieve
cardiomyopathie
Ernst van systolische en diastolische dysfunctie evalueren
o Pericardiaal lijden
Pericardiale effusie, tumor
Tamponade: diastolische collaps van rechter atrium
Constrictieve pericarditis
Cardiale katheterisatie
o Drukmeting
Linkerhart of aorta: katheter inbrengen in arteria femoralis of brachialis
Rechterhart en a. pulmonalis: vena femoralis, brachialis of jugularis
Structuur
Normale druk (mmHg)
Rechter atrium
2-8
Rechter ventrikel
15-30 / 2-8
Arteria pulmonalis
15-30 / 4-12
Wiggedruk
2-10
Linker atrium
2-10
Linker ventrikel
100-140 / 3/12
Aorta
100-140 / 60-90
8
o
o
Meting van de bloed flow
Thermodilutie methode: fysiologisch zout van een gekende temperatuur
wordt ingespoten in het rechter hart, de snelheid waarmee de temperatuur
stijgt wordt gemeten en hieruit kan de cardiac output berekend worden
Fick methode: cardiac output is gelijk aan zuurstof consumptie gedeeld door
arterioveneus verschil in zuurstofgehalte
Berekening van de vasculaire weerstand
Pulmonaire vasculaire weerstand: 𝑃𝑉𝑅 =
-
𝑀𝑃𝐴𝑃−𝐿𝐴𝑃
𝐶𝑂
× 80
MPAP = gemiddelde druk in a. pulmonalis (mmHg)
LAP = gemiddelde druk linker atrium (mmHg)
CO = cardiac output (L/min)
Systemische vasculaire weerstand: 𝑆𝑉𝑅 =
𝑀𝐴𝑃−𝑅𝐴𝑃
𝐶𝑂
× 80
MAP = gemiddelde arteriële druk (mmHg)
RAP = gemmidelde druk rechter atrium (mmHg)
o Contrast angiografie
Vooral gebruikt in angiografie van de coronairen
Mogelijkheid tot angioplastie of plaatsen van een stent
Nucleaire beeldvorming
o Myocardiale perfusie
Ischemie en infarctie door coronary artery disease detecteren
Thallium: opname bij inspanning (of na adenosine/dipyridamole) en in rust
Transient ischemische weefsels zullen in rust normale tracer opname
vertonen
Geïnfarcteerde weefsels zullen in rust nog altijd cold spots vertonen
Hibernerend myocard weefsel geeft ook cold spots zowel bij
inspanning als in rust, maar is nog metabool actief en kan
functionaliteit terugkrijgen als de bloed flow herstelt wordt
(chronische reductie van coronaire bloed flow)
(dien extra isotoop toe en maak een nieuwe opname om het
onderscheid te maken met permanent dysfunctioneel weefsel)
Technetium: fixeert in de cellen, geen redistributie na verloop van tijd
o Radionuclide ventriculografie (blood pool imaging)
Ventrikel functie analyseren
Radioisotoop gebonden aan rode bloedcellen of humaan serum albumine
Ventriculaire ejectiefractie ook rechts te meten (met echocardiografie enkel
links)
o Myocardiaal metabolisme
Petscan
Myocardiale perfusie: positron-emitting isotoop wordt in functie van de
bloed flow opgenomen door de myocyten
Myocardiale leefbaarheid: glucose verbruik, geïnfarcteerd weefsel vertoont
geen glucose opname, ischemisch weefsel en hibernerend weefsel
verhoogde glucose opname (revascularisatie zal verbetering van de perfusie
geven)
9
-
CT
o
o
-
o
MRI
o
Grote vaten (aortadissectie, aneurysma), pericardium (pericardvocht, verdikking,
calcificatie), myocardium (regionale hypertrofie, ventriculaire aneurysmata),
intracardiale trombusvroming en coronaire arteriën kunnen beoordeeld worden
Spiraal CT: pulmonaire embolisatie
Electron beam CT: snel, screenen voor coronary artery disease
Multidetector row CT
Nadelen: contrast, hoge stralingsbelasting, niet zo sensitief als angiografie, niet
geschikt voor evaluatie van stenose in stents
Voordelen: snel, relatief goedkoop, minder invasief dan angiografie
Grote vaten, congenitale afwijkingen, ventriculaire massa en volume, intravasclaire
trombus, cardiomyopathie en neoplastische afwijkingen kunnen beoordeeld worden
Coronary MRA: coronary artery disease, congenitale defecten in coronairen,
geen contrast nodig
Contrast-enhanced MRI: gadolinium contrast, concentreert zich in
geïnfarcteerd weefsel
10
Hoofdstuk 5
Atherosclerosis
-
-
Arteriële wand
o Intima: éénlagig epitheel, metabool actieve barrière
o Media: gladde spiercellen en extracellulaire matrix omgeven door elastine
o Adventitia: zenuwen, lymfevaten en vasa vasorum
Fysiologie
o Endotheelcellen
Produceren anti- en protrombotische moleculen, normaal netto antitrombotisch effect (heparaan sulfaat, trombomoduline, NO, prastacycline)
Produceren vasodilatoren (NO, prostacycline) en vasoconstrictoren
(endotheline), normaal netto relaxatie van de gladde spiercellen
Sommige endotheliale producten inhiberen de proliferatie van gladde
spiercellen in de intima
Normaal anti-inflammatoire eigenschappen, maar secreteren chemokines na
weefselschade of infectie
o Vasculaire gladde spiercellen
Worden gemoduleerd door vasoactieve stoffen (angiotensine II,
acetylcholine, endotheline, NO)
Produceren collageen, elastine en proteoglycanen die de vasculaire
extracellulaire matrix vormen
Kunnen vasoactieve en proinflammatoire mediatoren synthetiseren, die
mogelijk van belang zijn in de pathogenese van atherosclerose
o
-
Extracellulaire matrix
Zorgt voor sterkte en flexibiliteit van de vaten en regulatie van de spiercellen
erin
Atherosclerose
o Fatty streak: eerst zichtbare letsel, niet stenotiserend, zichtbaar vanaf 20 jaar
Endotheliale dysfunctie: door niet-laminaire flow (in sterk vertakte vaten) en
chemische factoren
Lipoproteine entry en modificatie: LDL accumulatie in de subendotheliale
ruimte (binding met proteoglycanen), oxidatie en glycolisatie van de LDL
geeft proinflammatoire vorm, promotie van de inflammatoire reactie
Leukocytenwerving: leukocyte adhesion molecules en chemoattractie,
voornamelijk monocyten en T-lymfocyten
Foam cell formatie: de monocyten die in de intima gedrongen zijn
differentiëren naar fagocyten en nemen de lipoproteïnen op om foam cellen
te vormen (niet via LDL-receptoren, die zijn onderdrukt door de hoge
cholesterol content en ze herkennen geen mLDL, maar via scavenger
receptoren geen inhibitie door negatieve feedback)
11
o
-
Plaque progressie
Migratie en proliferatie van gladde spiercellen in de intima, secretie van
extrecellulaire matrixmoleculen: vorming van stevige fibreuze kap
Platelet derive growth factor (uit foam cellen, bloedplaatjes en
dysfunctioneel epitheel) stimuleert dit proces en maakt de fibreuze
kap sterker net als andere groeifactoren
Inflammatie wordt in stand gehouden onder invloed van cytokines,
cytokines stimuleren ook de vorming van matrix metalloproteinases
(MMP) waardoor de fibreuze kap afgebroken wordt
Subklinische events (bijv. Intraplaque bloeding) kunnen een lokale
uitbarsting van gladde spiercel migratie en proliferatie geven, dus
géén graduele groei van de plaque
Vroeg: compensatoire outward remodeling van de arteriële wand (kan
angiografisch gemist worden)
Later: stenose, limitatie van de bloedflow en van de perfusie met ischemie
tot gevolg
o Plaque disruptie
Als de plaque groeit komt er meer hemodynamische stress te staan op de
‘schouder’ van de plaque, hier vindt ook accumulatie van foam cellen en Tlymfocyten plaats, waardoor dit een voorkeursplaats voor disruptie is
De balans van opbouw en afbraak van de fibreuze kap is nog belangrijker,
een fragiele kap zal eerder scheuren ook al is de stenose minder
uitgesproken dan bij een zeer stevige dikke kap
Een factor die bepaalt of een disruptie lijdt tot een transiënte, nietobstructieve trombus of een volledig occlusieve, is de balans tussen
coagulatie en fibrinolyse in het bloed, hoe meer het bloed neigt tot
coagulatie, hoe ernstiger de gevolgen van de disruptie zullen zijn
Complicaties van atherosclerose
o Calcificatie: de arteriële wand verandert in een soort stijve buis die zeer kwetsbaar is
o Ruptuur: trombusvorming die kan leiden tot infarcten
o Bloeding in de plaque: intramuraal hematoom verergert de stenose
12
o
-
Embolisatie: afgescheurde stukken van de plaque kunnen distale kleinere bloedvaten
occluderen
o Verzwakking van de arteriële wand: aneurysmavorming door atrofie en verlies van
elastisch weefsel
o Microneovascularisatie van de plaque: risico op bloeding en het verschaft extra
mogelijkheid tot aanvoer van leukocyten
Risicofactoren voor atherosclerose
o Niet-modificeerbare factoren
Hoge leeftijd
Mannelijk geslacht
Erfelijkheid
o Dyslipidemie
Target LDL < 100 mg/dl (bij zeer hoog risico op vasculaire events <70)
o Roken
Reversibel, na 3 jaar gestopt te zijn is het cardiovasculaire risico gelijk aan
niet-rokers
o Hypertensie
Hemodynamische stress zorgt voor endotheliale beschadiging en verhoging
van het aantal scavenger receptors op macrofagen (stimuleert de
ontwikkeling van foamcellen)
o Diabetes mellitus
Niet-enzymatische glycolisatie van LDL (mLDL wordt opgenomen door
scavenger receptoren)
Protrombotische en antifibrinolytische neiging van het bloed
Verminderde endotheliale functie
o Metabool syndroom
Hypertensie, hypertriglyceridemie, verminderd HDL, cellulaire insuline
resistentie, viscerale obesitas
o Sedimentaire levensstijl
Beweging heeft een gunstig effect op lipideprofiel, bloeddruk,
insulinesensitiviteit, endotheliale productie van NO
o Oestrogeenstatus
Oestrogenen beschermen tegen atherosclerose, vrouwen hebben voor de
menopauze een lager cardiovasculair risicoprofiel dan mannen, na de
menopauze is het gelijk
Nut en veiligheid van hormoontherapie is niet bewezen
o Biomerkers
Homocysteine: oxidatieve stress, vasculaire inflammatie en
bloedplaatjeshechting zijn verhoogd
Lipoproteine (a): variant van LDL
C-reactive protein en andere inflammatoire merkers: voorspelling CV risico
13
Hoofdstuk 6
Ischemic heart disease
-
Bloedvoorziening myocard; afhankelijk van
o Zuurstofgehalte in het bloed (hemoglobine concentratie en mate van systemische
oxygenatie, meestal vrij constant)
o Coronaire bloedflow (variabel), afhankelijk van perfusiedruk en vaatweerstand
In coronairen is de perfusiedruk het hoogst tijdens diastole, omdat de vaten
tijdens systole worden samengedrukt door het contraherende myocard
Zuurstofextractie is in basale omstandigheden al maximaal, dus elke
toename in vraag moet tegemoetgekomen worden door verhonging van de
bloedflow en hierbij is het verlagen van de vaatweerstand belangrijk
Metabole factoren: aeroob metabolisme wordt stilgelegd waardoor er
opstapeling van ADP/AMP ontstaat adenosine vasodilatatie (ook
lactaat, acetaat, protonen, CO2)
Endotheliale factoren: endotheelcellen kunnen vasodilatoren (NO,
prostacycline, EDHF) en vasoconstrictoren (endotheline 1) produceren, dit
wordt gestimuleerd door o.a. ACh, hemodynamische stress, hypoxie,
bloedplaatjes producten. Normaal gesproken ligt de balans bij vasodilatatie,
in dysfunctioneel endotheel verschuift de balans naar vasoconstrictie
Neurale factoren: α-adrenerge stimulatie vasoconstrictie,
β2-adrenerge stimulatie vasodilatatie
-
Zuurstofvraag myocard; afhankelijk van
o Ventriculaire wandspanning
-
𝑃×𝑟
2ℎ
𝜎=
o Hartslag
o Contractiliteit
Myocardiale ischemie in CAD wordt veroorzaakt door
o Stenose van de coronairen door atherosclerose
o
Vooral de kleinere diameter is van belang voor toegenomen weerstand
De weerstandsvaten (arteriolen) kunnen dilateren als compensatie van
atherosclerotische stenose in de proximale coronairen, pas bij een vernauwing van
>70% treedt er ischemie op bij inspanning en bij >90% in rust
Endotheeldysfunctie bij atherosclerose
Ongepaste vasoconstrictie
-
P = intraventrikulaire druk, r = ventrikel radius, h = wanddikte
Door verminderde afgifte van endotheliale vasodilatoren zoals NO wordt
het directe adrenerge effect niet tegengewerkt en is het netto effect
vasoconstrictie
Verlies van normale antitrombotische functie
o Hypotensie (verminderde perfusie druk)
o Sterk verminderde zuurstof content in het bloed (bijv. anemie)
o Zeer grote toename van zuurstofvraag (acute hypertensie, tachycardie, ernstige
aorta stenose)
Gevolgen
o Opstapeling metabole afvalproducten
14
-
AMP/ADP niet omgezet tot ATP verminderde pompfunctie congestief
longlijden met dyspneu
Lactaat, serotonine, adenosine activeren pijnreceptoren?
o Stunned myocardium: transiënte ischemie zonder necrose, maar toch na herstel van
de bloedflow nog systolische dysfunctie die gadueel herstelt (calcium overload en
opstapeling van vrije radicalen)
o Hibernating myocardium: chronische ventriculaire dysfunctie door een chronisch
verminderde bloedaanvoer, herstel van de bloedflow geeft direct herstel van de
functie
o Ischemische syndromen
Stabiele angina
Onstabiele angina: wanneer stabiele angina progressie begint te vertonen,
voorbode van myocard infarct
Variant angina of Prinzmetal angina: veroorzaakt door vasospasmen, kan in
rust voorkomen (atherosclerotische lesies (nog) niet aanwezig, enkel
endotheeldysfunctie)
Silentieuze ischemie
Syndroom X: typische angina klachten (niet in rust) maar geen
atherosclerose
Chronische stabiele angina
o Anamnese
Eerder druk op de borst, oncomfortabel, zwaar of branderig gevoel dan pijn
Ongeveer 1 tot 10 minuten durend
Diffuus, maar meestal retrosternaal gelokaliseerd (kan ook rug, arm, nek,
onderkant van het gezicht of bovenin het abdomen zijn!, vaak radiatie naar
(linker) schouder en arm)
Beweging of ademhaling hebben geen invloed op de pijn
Kan gepaard gaan met tachycardie, zweten, nausea, dyspneu, moeheid en
zwakte
Vooraf gegaan door fysieke of emotionele stress, grote maaltijd, koud weer
(tenzijn variant angina)
Snelle verbetering bij inname van nitroglycerine
Preventieve vermindering van de dagelijkse activiteit om aanval te
voorkomen
Cardiovasculair risicoprofiel
Dd. andere cardiale, gastrointestinale of musculoskeletale oorzaken
o Klinisch onderzoek
Zo mogelijk tijdens aanval
HR en BD gestegen
S4 gallop tijdens atriale contractie
Carotide geruis of afgenomen pols in extremiteiten kan wijzen op
atherosclerotische problematiek
o Diagnose
ECG tijdens aanval (ST segment en T wave veranderingen): normalisatie
wanneer de klachten oplossen (i.t.t. bij MI), buiten aanval kan de ECG
15
-
normaal zijn of wijzen of een ooit doorgemaakt MI dat wijst wel indicatie
geeft voor onderliggende CAD
Stress ECG: door inspanning of farmacologsich geinduceerd (bij diagnostisch
doeleinde medicatie stoppen voor test, bij opvolging niet)
Nucleaire beeldvorming, tijdens stress en in rust om geinfarceerde weefsels
te onderscheiden van transient ischemische weefsels
Inspannings echocardiografie tijdens stress en in rust
Coronaire angiografie, gouden standaard voor diagnose maar invasief
CT met contrast, minder sensitief dan angiografie
o Verloop
Stabiele angina kan jaren lang stabiel blijven of overgaan in acuut coronair
syndroom (onstabiele angina, myocard infarct) of plotse dood
Factoren van prognostisch belang zijn locatie en ernst van stenose, ernst van
linkerventrikel dysfunctie, inspanningstolerantie en ernst van de symptomen
Behandeling
o Doel
Anginale episodes verminderen
Acuut coronair syndroom vermijden
Overleving vergroten
o Leefstijlveranderingen: risicoreductie
o Farmacologisch
Acuut: sublinguaal nitroglycerine (effect binnen 2 minuten)
Preventie anginale episodes: organische nitraten, β-blokkers, calciumkanaal
blokkers (deze middelen hebben geen effect op het atheroscleroische proces
en vergroten de overleving niet!)
Preventie acuut cardiaal syndroom/plotse dood: antiplaatjes therapie
(aspirine, clopidogrel), lipide regulerende therapie (statines), ACE inhibitoren
o Revascularisatie
Indicatie:
Geen respons op farmacologische therapie
Onacceptabele neveneffecten farmacologische therapie
Hoog-risico CAD (>50% stenose van LAD, multivessel + verminderde
linkerventrikelfunctie)
PCI (Percutane coronaire interventie)
PTCA (percutane transluminale coronaire angioplastie),
ballonkatheter ingebracht door perifere arterie, door hoog risico op
recidive zijn coronaire (drug-eluting) stents ontwikkeld
GABG (coronaire arteriële bypass graft)
Veneuze graft (v. saphena) geplaatst vanaf aorta basis naar een
aangetaste coronair distaal van de stenose (kwetsbaar voor
versnelde atherosclerose)
Arteriële graft (a. mammaria interna) houdt zijn origine en eindigt op
de aangetaste coronair distaal van de stenose (alleen mogelijk op
LAD vanwege afstand)
16
Hoofdstuk 7
Acute coronary syndromes
-
-
In 90% van de gevallen veroorzaakt door plaque eruptie met intracoronair trombus tot
gevolg
o Partiële occlusie
Onstabiele angina (geen myocardiale necrose)
Non-ST-elevation myocardial infarction of NSTEMI (wel myocardiale necrose)
o Volledige occlusie
STEMI
Hemostase
o Primair: bloedplaatjes
o Secundair: fibrine
o Endogene antitrombotische mechanismen voorkomen spontane trombose en
occlusie
-
Niet-atherosclerotische oorzaken van ACS
o
o
o
o
o
o
o
o
-
-
Deactivatie van stollingsfactoren (antitrombine, proteïne C/S, trombomoduline,
TFPI)
Lyse van fibrine klonters (tPA)
Bloedplaatjes inhibitie en vasodilatatie (prostacycline en NO)
Vasculitis syndromen
Coronaire embolisatie
Congenitale abnormaliteit
Trauma of aneurysma
Vasospasmen
Verhoogde viscositeit van het bloed
Spontane dissectie van coronaire arterie
Sterk verhoogde zuurstof vraag van myocard
Onstabiele angina onderscheid zich van MI doordat er geen sprake is van necrose, door
toenemende sensitiviteit van testen wordt deze groep steeds kleiner, misschien bestaat ze
in de toekomst helemaal niet meer
Myocard infarct
o NSTEMI / STEMI
o Transmuraal infarct: omvat de volledige dikte van het myocard
o Subendocardiaal infarct: omvat enkel de binnenste lagen van het myocard
o Vroege veranderingen bij infarct: verminderde functie na 2 minuten
Shift van aeroob naar anaeroob metabolisme pH↓
Tekort aan ATP inhibeert de Na+-K+-pomp
IC Na+ ↑ intrecellulair oedeem
EC K+↑ risico aritmieën
Irreversibele schade begint na 20 minuten
Membraan defecten: proteolytische enzymen lekken uit myocyten
en beschadigen het naburige myocardium
Myocardiaal oedeem ontwikkelt zich na 4 tot 12 uur
Histologisch: wavy myofibers
Acute inflammatoire respons na 4 uur (neutrofielen)
17
-
Coagulatie necrose na 18-24 uur (pyknotische kernen en eosinofiel
cytoplasma)
o Late veranderingen bij infarct
Verwijderen van necrotisch myocard door fagocyten
Collageendepositie voor littekenvorming (compleet na 7 weken)
Ventrikulaire remodeling ( kamergrootte en wanddikte)
Presentatie
o Onstabiele angina
Te onderscheiden van stabiele angina door een van de volgende zaken:
Crescendo patroon in frequentie, duur en of intensiteit van angina
Angina in rust
Nieuwe onset van hevige anginale episodes zonder andere
symptomen van CAD
o Acuut myocardinfarct
Symptomen gelijk angina, maar meestal heviger, langer durend en met meer
uitstraling (nek, kaak, schouders, armen)
Verminderd niet met rust en weinig respons op sublinguaal nitroglycerine
Tot 25% van de patiënten is asymptomatisch (vaak bij diabetes)
Sympatisch systeem respons: zweten, tachycardie en een koele, klamme
huid door vasoconstrictie
Parasympatisch effect: nausea, overgeven en zwakte
Lichte koorts
Dyspneu
S4 gallop, systolisch geruis
Differentiaal diagnose
-
Diagnose
o Klinisch
o ECG
ST- depressie en/of inverse T-golven bij onstabiele angina (transiënt) en
NSTEMI (persiterend)
ST-elevatie na enkele uren gevolgd door T-golf inversie en Q-golven bij STEMI
o Serum markers voor necrose: aanwezig bij STEMI / NSTEMI
-
Pericarditis: wrijvingsgeruis, pijn variabel met ademhaling en positie
Aorta dissectie: scheurende pijn die migreert, assymetrie in brachiale
bloeddruk
Pulmorair embool: pleuritis pijn en pleuraal wrijfgeruis
Pneumonie: pleuritis pijn, hoest, sputum, abnormale longauscultatie
Pneumothorax: pleuritis pijn en abnormale longausultatie
Oesophagaal spasme: gerelateerd aan slikken
Acute cholecystitis: nausea, geschiedenis van voedsel intolerantie
Troponine, te detecteren van 3-4 uur tot 10-14 dagen na het MI, voorkeursmarker
Creatine kinase, te detecteren van 3-8 uur tot 48-72 uur na MI, minder sensitief en
specifiek
o Echocardiografie
Behandeling
o Patiënt opnemen en in monitoring situatie brengen
18
o
UA / NSTEMI
Anti-ischemische therapie
β-blokkers, inhiberen sympatische signalen naar het myocard
Nitraten, verminderen verneuze retour door venodilatatie
Nonhydropyridine Ca2+ kanaal antagonisten (diltiazem, verapamil), negatief
inotroop en chronotroop effect, enkel aangewezen bij patiënten bij wie
ischemie persisteert na β-blokkers en nitraten of bij contra-indicatie voor βblokkers
Antitrombotische therapie
Antiplaatjestherapie (aspirine, clopidogrel)
Anticoagulerende therapie (heparine)
o
-
STEMI
Medicatie
Aspirine en/of clopidogrel
Heparine
β-blokkers
IV nitraten
Revascularisatie
Fibrinolytische therapie (bloedingsrisico)
PCI (percutane coronaire interventie)
o Bijkomende behandeling
ACE-remmers (bij LV dysfunctie)
Statines
Complicaties
o Herval (postinfarct angina is een slecht teken met verhoogd risico op herinfarctie)
o Aritmieën veroorzaakt door slechte perfusie exciteerbaar weefsel, accumulatie van
toxische metabolieten, autonome stimulatie of toegediende aritmogene medicatie
o
o
o
o
o
o
Ventriculaire fibrillatie: hoofdverantwoordelijk voor plotse dood prehospitaal
Supraventriculaire aritmieën
Conductie blocks
Congestief hartfalen veroorzaakt door systolische en diastolische ventrikeldysfunctie
Geef diuretica + β-blokker + ACE inhibitor
Cardiogene shock (zwaar verminderde cardiac output en hypotensie)
Geef intra aortische ballon pomp of percutane LVAD
Rechter ventrikelinfarctie geeft rechter hartfalen met hypotensie
Geef intraveneuze infusie
Mechanische complicatie
Papillaire spier ruptuur mitralis regurgitatie
Ventriculaire wand ruptuur of pseudoaneurysma (lethaal of gevaar voor
scheuren of tamponade)
Ventriculair septum ruptuur left-to-right shunt met congestief hartfalen
Ventriculair aneurysma (weken tot maanden na MI) perifere embolisatie,
ventriculaire ritmestoornissen of hartfalen door verminderde cardiac output
Pericarditis (scherpe pijn, koorts en een pericardiaal wrijfgeruis)
Dressler syndrome: laattijdige pericarditis, mogelijk immuun gemedieerd
Tromboembolisatie veroorzaakt door hemostase in de kamers
19
Hoofdstuk 8
Valvular heart disease
-
-
Reumatische koorts
o Vroeger de meest frequente oorzaak van kleplijden, tegenwoordig zeldzaam
o Inflammatoire ziekte die het hart, de huid en bindweefsel aantast
o Complicatie van streptokokken infecties in de bovenste luchtwegen
o De carditis kan zowel pericard, myocard als endocard beslaan
o Kan permanente vervorming en verslechtering van de hartkleppen veroorzaken na
lange latente periode
o Symptomen
Koorts
Rillingen
Moehied
Migrerende arthralgieën
o Jones criteria voor de diagnose van reumatische koorts
Bewijs van streptokokken infectie
2 van de majeure criteria
Carditis
Polyarthritis
Onvrijwillige beweginen
Erythema marginatum (uitslag met uitbreidende randen)
Subcutane nodules
OF 1 majeur criterium en 2 mineure criteria
Migrerende arthralgieën
Koorts
Verhoogde inflammatoire parameters
Verlengd PR interval op ECG
o Behandeling: aspirine, penicilline, behandeling van de complicaties
o Bij chroniciteit grote kans op stenose of regurgitatie van de hartkleppen (vnl mitralis)
Mitralisklep stenose
o Oorzaken
Reumatische koorts
Congenitale abnormaliteit
Calcificatie van de annulus mitralis bij ouderen
Endocarditis
o Pathofysiologisch zien we verdikte of gecalcificieerde kleppen, vergroeien van de
commisuren en verdikking / verkorting van de chordae tendinae
o Abnormale drukgradiënt tussen linker atrium en linker ventrikel
o Hemodynamisch significante MS heeft een valvulaire diameter van minder dan 2 cm²
o ↓ stroke volume en cardiac output
o Hoge drukken in de pulmonaire circulatie longoedeem dyspnoe, hemoptysis (=
passieve pulmonaire hypertensie)
o Reactieve pulmonaire hypertensie: beschermingsmechanisme, verhoogde
arteriolaire weerstand zodat dat hydrostatische druk in de longen vermindert, kan op
20
-
lange termijn echter voor rechterhartfalen zorgen door verhoogde druk in het
rechter atrium (opgezette jugulaire venen, hepatomegalie, ascites, perifeer oedeem)
o Dilatatie van het linker atrium atriale fibrillatie ↓ duur diastole en cardiac output
o Relatieve stase in linker atrium trombus formatie met perifere embolisatie
o Complicaties: infectieve endocarditis, zie voorgaand vetgedrukt
o Auscultatie
S1 in het begin luid, later normaal tot verminderd als ze klepbladen zo dik en
gecalcifieerd zijn dat ze immobiel zijn geworden
Opening snap bij het openen van de mitralis klep te horen
Diastolisch decrescendo geruis met pre-systolische accentuatie
o Belangrijkste diagnostische onderzoek is echocardiografie
o Behandeling
Diuretica (vasculaire congestie)
β-blokker, verapamil/diltiazem of digoxine (atriale fibrillatie)
Chronische anticoagulantia (tromboembolisatie)
Percutane ballon mitralis valvuloplastie (evt. residueel atriaal septum defect)
Open mitralis commisurotomy of mitralis klep vervanging
Mitralisklep regurgitatie
o Oorzaken
Structurele abnormaliteiten van de annulus mitralis, klepbladen, chordae
tendinae of papillair spiertjes
Infectieve endocarditis
Reumatische koorts (excessieve verkorting van de chordae tendinae met
retractie van de klepbladen)
Hypertrofische obstructieve cardiomyopathie
Calcificatie van de annulus mitralis bij ouderen (zeker bij hypertensie,
diabetes of eind-stadium nierfalen)
Idiopatische ruptuur van de chordae tendinae
Linker ventriculaire dilatatie
o Een deel van de ventriculaire output gaat terug in het linkeratrium tijdens systole
↑ linker atriaal volume en druk, ↓ forward cardiac output, volume gerelateerde
stress op het linker ventrikel
o Acuut
o
Weinig compliantie van het linker atrium drukstijging pulmonaire congestie en
oedeem (passieve pulmonaire hypertensie)
Verhoging van het stroke volume zodat het linker ventrikel volume normaal blijft
Chronisch
Compliance van het linker atrium dilatatie, normale atriale druk en weinig
pulmonaire problematiek
Ventriculaire ejectie meer geneigd naar het compliante linker atrium ten opzichte
van de aorta ↓ cardiac output vermoeidheid en zwakte
Linker atrium dilatatie is predispositionerend voor atriale fibrillatie
Excentrische hypertrofie van het linker ventrikel
↑ stroke volume houdt de cardiac output lang op normaal niveau, maar de
ventriculaire functie gaat langzaamaan achteruit tot hartfalen
21
o
-
-
Ausculatatie
Apical pansystolisch geruis
Bij het samenknijpen van de vuist zal de intensiteit van het geruis toenemen
S3, verhoogde volume input in ventrikel tijdens diastole, kan gehoord worden
Apicale beat verplaatst naar lateraal vanwege ventriculaire hypertrofie
o Behandeling
Acuut
i.v. diuretica
vasodilatatie
Chronisch
Mitralisklep herstel of vervanging
Mitralisklep prolapse
o Klepbladen puilen uit in het linker atrium tijdens ventriculaire systole
o Meestal asymptomatisch, kan samengaan met mitralis regurgitatie
o Kan autosomaal dominant overgeërfde aandoening zijn of deel uitmaken van een
andere bindweefselziekte zoals syndroom van Marfan
o Diagnose op echocardiografie
o Prognose normaal goed, follow-up voor regurgitatie
Aortaklep stenose
o Oorzaken
Calcificatie bij ouderen
Congenitaal afwijkende kleppen (bicuspide aortaklep)
(Reumatisch kleplijden)
o Hemodynamisch significante AS heeft een afname in valvulaire diameter van >50%
o Compenserende concentrische ventrikel hypertrofie om de hoge druk aan te kunnen
o ↓ Compliantie ventrikel ↑ ventriculaire druk in diastole atrium hypertrofie
risico atriale fibrillatie
o Symptomen
Angina
Verhoogde spiermassa (hypertrofie) en wandspanning vragen meer
zuurstof
Verhoogde diastolische ventriculaire druk vermindert de coronaire
perfusie druk gradiënt, dus minder zuurstof aanvoer
Inspanningsgebonden syncope
Perifere vasodilatatie en onvermogen om de cardiac output te
verhogen bij inspanning ↓ cerebrale perfusie druk
Congestief hartfalen
Pas wanneer de linker ventrikelfunctie begint te falen en de hoge
afterload niet mer goed aankan, zal de druk in het ventrikel en
daarmee in het atrium gaan stijgen pulmonaire congestie
o Eens symptomatisch, is de prognose zeer slecht
o Behandeling: klepvervanging
22
-
-
-
Aortaklep regurgitatie
o Oorzaken
Abnormaliteiten van de klepbladen
Congenitaal (bicuspiede klep)
Endocarditis
Reumatisch
Dilatatie van de aorta wortel
Aneurysma
Aorta dissectie
Syphilis
o ↑ druk in het ventrikel door terugstroom vanuit aorta in diastole ↑ stroke volume
o Acuut
Ventrikel normaal in grootte en niet compliant ↑ diastolische druk
↑ ook in atrium pulmonair oedeem en dyspneu
o Chronisch
Compensatie van het ventrikel aan de hoge volume load excentrische
hypertrofie weinig drukverhoging en pulmonaire problematiek
↓ aortische = systemische diastolische bloeddruk (↓coronaire perfusie druk)
↑ stroke volume en dus systolische bloeddruk
↑ polsdruk (=verschil tussen boven- en onderdruk)
o Symptomen en klinische tekens
Dyspneu bij inspanning
Moeheid
Verminderde inspanningstolerantie
Gevoel van grote hartarbeid
Vergrote polsdruk
Decrescendo diastolisch geruis
o Behandeling
Asymptomatisch monitoring ventrikel functie
Calcium kanaal blokkers of ACE inhibitors (hypertensie)
Chirurgische correctie
Tricuspidaalklep stenose
o Zeldzaam
o Veroorzaakt door reumatische koorts
o Valvuloplastie of klepvervanging
Tricuspidaalklep regurgitatie
o Oorzaken
Rechter ventrikel dilatatie
Reumatisch
Carcinoid syndroom (serotonine metabolieten gesecreteerd door neuroendocriene tumoren vormen cardiale plaques in het rechterhart)
o Klinische tekenen
Prominente v-wave in jugulaire venen
Pulserende lever
Systolisch geruis dat luider wordt bij inspiratie
23
o
-
-
-
Behandeling van de onderliggende oorzaak van de rechter ventrikel dilatatie +
diuretica
Pulmonaalklep stenose
o Zeldzaam
o Veroorzaakt door congenitaal misvormde klepbladen
o Transkatheter ballon valvuloplastie
Pulmonaalklep regurgitatie
o Veroorzaakt door ernstige pulmonaire hypertensie
Prosthetische kleppen
o Mechanisch of biologisch
o Mechanische kleppen blijven langer goed, geen scheuren of calcificaties van de
kleppen
o Biologische kleppen veroorzaken minder trombo-embolisatie (langdurige
behandeling met anti-coagulantia is niet noodzakelijk) en minder infectie risico
Infectieve endocarditis
o Classificatie
Klinisch
Acute bacteriële endocarditis, bijv. S. aureus (vaker in stedelijke
gebieden met hogere prevalentie van intraveneus drugsgebruik)
Subactute bacteriële endocarditis, minder fulminant, bijv. S. viridans
Afhankelijk van substraat
Natuurlijke klep endocarditis
Prosthetische klep endocarditis
Endocarditis in de setting van acuut drugs misbruik
Afhankelijk van specifieke microbe
o Pathogenese
Beschadiging van het endocardiaal oppervlak
Trombus formatie aldaar
Bacteriën in de circulatie
Bacteriële aankleving aan het beschadigde endocardiale oppervlak
o Meest voorkomende oorzaak is turbulente bloed flow door onderliggend kleplijden
o Continuerende bacteriëmie kan leiden tot
Mechanische cardiale schade
Trombotische of septische embolen
Schade door antigen-antilichaam (immuncomplexen) depositie
o Symptomen en klinische tekenen
Hoge koorts met rillingen bij acute endocarditis
Meer nonspecifieke symptomen bij subacute endocarditis (moeheid,
anorexie, zwakte, myalgie, nachtzweten)
Geruisen die wijzen op kleplijden
Mogelijke gevolgen van septische embolisatie of immuuncomplexen
depositie (neurologische bevindingen, nierschade)
Perifere stigmata (petechiae, splinterbloedingen)
24
o
o
Diagnose door middel van Duke criteria (positief als 2 major, 1 major + 3 minor of 5
minor criteria voldoen)
Major criteria
Positieve bloed cultuur (minstens 2 aparte bloednames, typische of
persisterende aannemelijke micro-organismen)
Bewijs van endocardiale betrokkenheid (trans-oesofageale
echocradiogram of nieuw kleplijden)
Minor criteria
Voorbeschikkende cardiale afwijking of intraveneuw drugsgebruik
Koorts vanaf 38°c
Vasculaire fenomenen
Immunologische fenomenen
Positieve bloedculturen die niet voldoen aan de major criteria
Behandeling
4-6 weken hoge dosis intraveneuze antibiotica
Heelkundige interventie met meestal klepvervanging voor antibiotica
resistente problematiek, ernstige klepinsufficiëntie met hartfalen,
myocardiale abcessen en herhaaldelijke trombo-embolische events
Preventief antibiotica toedienen bij vatbare patiënten bij tandheelkundige
ingrepen, bovenste luchtweg ingrepen met incisie of biopsie van de
mucosae, genito-urinaire ingrepen bij aanwezig infectie of ingrepen aan
geïnfecteerd huid- of musculoskeletaal weefsel
25
Hoofdstuk 9
Heart failure
-
-
-
-
-
Forward failure: het hart kan niet genoeg bloed rondpompen om aan de metabole eisen van
het lichaam te voldoen
Backward failure: het hart kan enkel genoeg bloed rondpompen wanneer de cardiale
vullingsdruk abnormaal hoog is
Experimentele observaties
o Uitgerekte myocardvezels kunnen sterkere contracties tot stand brengen door de
interactie tussen actine en myosine te optimaliseren met meer cross bridges een
doordat de sensitiviteit van myofilamenten voor calcium verhoogt
Frank-Sterling: hoe hoger de preload hoe hoger de ventriculaire output
o De druk die door het ventrikel wordt gegenereerd en het eind-systolisch volume zijn
afhankelijk van de afterload
o Contractiliteit is naast vezel uitrekking en afterload nog afhankelijk van chemische of
hormonale invloeden
Hoe hoger het drukverschil is in verhouding tot het volume verschil bij het vullen van een
hartkamer, hoe minder compliant deze kamer is
Wet van La Place: 𝜎 =
𝑃×𝑟
2ℎ
o σ = wandspanning
o P = ventriculaire druk
o R = ventriculaire kamer radius ( v̴ olumetoename)
o h = wanddikte ( h
̴ ypertrofie)
Stroke volume en eind systolisch volume worden bepaald door
o Preload (hoe hoger de preload, hoe hoger SV, ESV blijft gelijk)
o Afterload (hoe hoger de afterload, hoe lager SV, hoe hoger ESV)
o Contractiliteit (hoe hoger contractiliteit, hoe hoger SV, hoe lager ESV)
Ejectiefractie
o Stroke volume / eind diatolisch volume
o Bij systolische dysfunctie is EF meestal verminderd
o Bij diastolische dysfunctie is EF meestal behouden
Systolische dysfunctie: verminderde capaciteit om bloed voort te pompen vanwege
verminderde contractiliteit of verhoogde afterload
Rechter hartfalen wordt meestal veroorzaakt door ↑afterload (pulmonaire hypertensie)
vanwege linker hartfalen
Neurohormonale compensatoire systemen bij hartfalen
o Verhogen de systematische vaculaire weerstand (TPR) zodat de bloeddruk op pijl
blijft bij een daling van cardiac output (𝐵𝑃 = 𝐶𝑂 × 𝑇𝑃𝑅 ) en zorgen voor water en
zout retentie ↑intravasculair volume ↑preload ↑SV
Adrenerg systeem
Baroreceptoren in de carotiden en aortaboog
Renine-angiotensine-aldosterone systeem (RAAS)
Verminderde renale perfusie + juxtaglomerulaire β2-receptoren
(adrenerg systeem)
Antidiuretisch hormoon (ADH) productie
26
-
-
Ventriculaire hypertrofie en remodeling
o Compensatoir mechanisme: wandspanning is in hartfalen vaak verhoogd door linker
ventrikel dilatatie en hoge intraventriculaire druk ventriculaire hypertrofie
vergroot de wanddikte en brengt zo de wandspanning naarbeneden
o Nadeel hiervan is de verminderder compliantie van het ventrikel nog hogere
intraventriculaire druk met pulmonaire hypertensie tot gevolg
o Volume overload excentrische hypertrofie (wanddikte vergroot in proportie met
de kamer radius)
o Pressure overload concentrische hypertrofie (enkel wanddikte vergroot waardoor
wandspanning verlaagt)
Hartfalen kan veroorzaakt worden door het verlies van myocyten (necrose of apoptose) of
het verlies van functie van levende myocyten
Symptomen van chronische hartfalen
o Linkerhartfalen
Dyspneu en tachypneu
Orthopneu
Paroxysmale nocturnale dyspneu en nachtelijk hoesten
Moeheid en zwakte
Verminderde urine output gedurende de dag met nocturie
Verminderde cerebrale perfusie afgevlakte mentale status
Hemoptyse
Diaforese
o Rechterhartfalen
Perifeer oedeem en gewichtstoename
Hepatomegalie met abdominaal ongemak
Opgezette jugulaire venen
27
-
-
Behandeling
o Verminderde ejectiefractie
Identificatie en behandeling van de onderliggende oorzaak (klepchirurgie,
revascularisatie, antihypertensieve therapie, alcoholstop)
Eliminatie van uitlokkende factoren (infectie, aritmie, overmatige
zoutinname, bepaalde medicatie)
Symptomatische behandeling (natrium restrictie + diuretica tegen congestie,
vasodilatatie + positieve inotropica om forward cardiac output te verhogen)
Modulatie van de neurohormonale respons om ventriculaire remodeling te
voorkomen en progressie van ventikeldysfunctie te vertragen
Verlengen van de overleving
Diuretica ↓veneuze retour / preload ↓pulmonaire congestie
ACE inhibitoren (of andere vasodilatoren)
Inotropica (β mimetica) ↑contractiliteit
β-blokkers controversieel
Aldosterone antagonisten gaan ventrikulaire remodeling tegen
Chronische anticoagulantia
Behandeling tegen aritmieën
o Behouden ejectie fractie
Behandelen van pulmonaire / systemische congestie
Diuretica
Behandelen van de onderliggende oorzaak van de diastolische dysfunctie
Symptomen van acuut hartfalen
o Urgente en levensbedreigende symptomatologie
o Klassificatie
Pressure overload aanwezig of niet (‘nat’ vs. ‘droog’)
Verminderde cardiac output of niet (‘koud’ vs. ‘warm’)
Warm en droog: normale hemodynamiek (andere oorzaak zoeken)
Warm en nat: acuut pulmonair oedeem, behouden weefselperfusie
Koud en nat: acuut pulmonair oedeem, verminderde weefselperfusie
Koud en droog: verminderde cardiac output maar geen congestie
(volume depletie)
o Longoedeem onstaat bij een wiggedruk vanaf 25 mmHg
Lasix (=furosemide) ↓preload
Morfine ↓angst, venodilatatie
Nitraten ↓preload
Oxygen
Positie: rechtop zitten om pooling van het bloed in het onderste deel van het
lichaam te faciliteren
28
Hoofdstuk 10
The cardiomyopathies
-
-
Groep van hart aandoeningen die primair veroorzaakt zijn door een structurele afwijking in
het myocard
Gedilateerde cardiomyopathie (uitgesproken ventrikel dilatatie, weinig hypertrofie)
o Meestal idiopathisch, zeer veel genetische, inflammatoire, toxische of metabole
oorzaken mogelijk
Acute virale myocarditis, meestal zelf limiterend, soms progressief naar
gedilateerde cardiomyopathie
Alcoholische cardiomyopathie, potentieel reversibel
Peripartum cardiomyopathie, presenteert met symptomen van hartfalen van
1 maand voor tot 6 maanden na bevalling
Familiale vormen zijn misschien verantwoordelijk voor een groot deel van de
idiopatische vormen
o Pathofysiologie
Dilatatie van alle vier kamers of eenzijdig
Verminderde contractiliteit ↓SV en CO
Neurohormonale compensatoire activiteit ↑heart rate en contractiliteit
(buffer voor CO)
↓renale bloedflow renine secretie door nier RAAS
↑vasculaire weerstand (angiotensine II) en intravasculair volume
(aldosteron) ↑afterload pulmonaire en systemische congestie
Chronisch verhoogd angiotensine II en aldosteron zorgen ook voor
pathologische myocard remodeling en fibrose
Kamer dilatatie zorgt voor mitralis- / tricuspidalisregurgitatie
o Eerst klachten zijn meestal gewichtstoename en kortademigheid bij inspanning
o Diagnose op echocardiografie
o Behandeling
Hartfalen: zoutrestrictie, diruretica, ACE inhibitors / angiotensine II receptor
blokkers, β-blokkers
Aritmieën: elektrolyten opvolgen, implantable cardioverter-defibrillator (ICD)
plaatsen, cardiac resychronization therapy
Trombo-embolisatie risico: orale onticoagulantia (systemische
anticoagulantia bij zeer hoog risico)
Cardiale transplantatie
Hypertrofische cardiomyopathie
o Asymetrische linker ventrikel hypertrofie, niet veroorzaakt door chronische pressure
overload
o Autosomaal dominant overgeërfde aandoening
o Pathofysiologie
Ventriculaire hypertrofie ↓compliance en diastolische relaxatie
↑diastolische druk met pulmonaire congestie
Wanordelijke histologie abnormale diastolische stijfheid en artimieën
29
-
Outflow obstructie (30%): vernauwing tussen de hypertrofische ventriculaire
septum en het anterieure blad van de mitralisklep, door de snelle ejectie
wordt het klepblad tegen het septum aangetrokken waardoor er een
obstructie van de bloedflow richting aorta ontstaat
Mitralis regurgitatie verergert de pulmonaire congestie
o Symptomen
Asymptomatisch
Dyspneu
Angina (hoge zuurstof vraag en nauwe coronairen in de hypertrofe massa)
Syncope door aritmieën of inspanning
Orthostatische duizeligheid
Plotse dood door aritmieën (ventriculaire fibrillatie)
o Behandeling
β-blokkers ↓heart rate en contractiliteit
calcium kanaal blokkers ↓ventriculaire stijfheid
Antiaritmica ( bv. Amiodarone)
ICD bij hoog risico
Myomectomie of percutane septale ablatie bij farmacoresistentie
Restrictieve cardiomyopathie
o Abnormaal stijve ventrikels met diastolische dysfunctie maar meestal vrij normale
systolische functie
Idiopatisch
Scleroderma
Amyloidose / sarcoidose
Stapelingsziektes
Endomyocardiale ziekte (fibrose, metastases, radiotherapie)
o Tekenen van links- en rechtszijdig hartfalen
o Te differentieren van constrictieve pericarditis (dat mogelijk reversibel is) door
biopsie, CT of MRI
o Behandeling
Onderliggende oorzaak behandelen
Zout restrictie en voorzichtig gebruik van diuretica
Soms orale anticoagulantia
30
Hoofdstuk 11
Mechanisms of cardiac arrhythmias
-
-
Veranderde impulsvorming
o Veranderde automaticiteit
Hartslag wordt verhoogd door sympathische stimulatie (stress) en verlaagd
door parasympathische stimulatie (rust) van de sinus knoop
Als de sinusknoop wordt onderdrukt kan impuls vorming door latente
pacemakers worden uitgevoerd escape beat, escape rhythm
(bescherming tegen bradycardie)
Latente pacemakers kunnen ook de controle over impuls vorming
overnemen door zelf een intrinsieke depolarisatie snelheid te ontwikkelen
die sneller is dan de sinusknoop ectopische hartslag (tachycardie)
o Abnormale automaticiteit
Myocardiale cellen buiten het geleidingssysteem kunnen automaticiteit
verkrijgen na weefselschade
o Getriggerde activiteit
Vroege nadepolarisatie: tijdens repolarisatiefase van een actiepotentiaal
(meer voorkomend bij lang QT syndroom of QT verlengende farmaca), kan
leiden tot een serie van depolarisaties (tachycardie) en torsades de pointes
Uitgestelde nadepolarisatie: volgt op een afgeronde actiepotentiaal (meer
voorkomend bij hoog intracellulair calcium zoals bij digitalis intoxicatie of bij
sterke catecholamine stimulatie)
Veranderde impuls geleiding
o Conductie blok: impuls wordt geblokeerd door niet-exciteerbaar weefsel (vanwege
ischemie, fibrose, inflammatie, farmaca)
Leidt tot bradycardie
Functionele blok: refractaire periode
AV-blok neemt overdrive suppressie weg waardoor de distale latente
pacemakers hun eigen ritme zullen aannemen (escape rhythm)
Beangrijkste reden voor het plaatsen van een permanente pacemaker
o Unidirectionele blok met reëntry
Leidt juist tot tachycardie
De tijd die het kost voor de imuls om door de reëntry-loop te reizen moet
groter zijn dan de refractaire periode, zodat de impuls niet onderbroken
wordt (conductie snelheid moet in praktijk gedaald zijn)
Wolff-Parkinson-White syndroom: er is een accesoire pathway tussen een
atrium en ventrikel waardoor er bij een juist getimede abnormale impuls een
mooie reëntry-loop beschikbaar is
31
-
Antiaritmische therapie
o Bradycardie
Elektronische pacemaker
Tijdelijk (in afwachting van permanente of voor transiënte
bradycardie)
o Externe transthoracale pacemaker (pijnlijk, enkel urgente
setting)
o Transveneus (pijnloos, risico op infectie en trombose door
katheter)
Permanent: registreren de cardiale activiteit en stimuleren enkel
wanneer nodig
Medicatie
Anticholinergica (bv. atropine iv)
β1-mimetica (bv. isoproterenol iv)
o Tachycardia
Medicatie
Antiaritmica zijn niet zonder gevaar, ze kunnen overdreven
bradycardie uitlokken of toxische non-cardiale neveneffecten geven
Vagotone maneuvres (bv. sinus carotis massage)
Elektrische cardioversie en defibrillatie
Externe cardioversie (gesynchroniseerd met QRS) of defibrillatie
(ongesynchroniseerd vanwege afwezigheid van georganiseerde QRS)
ICD
Katheter ablatie: via radiofrequentie kunnen reëntry circuits of weefsels met
abnormale automaticiteit vernietigd worden
32
Hoofdstuk 12
Clinical aspects of cardiac arrhythmias
-
Bradyaritmieën
o <60 bpm
o Sinus bradycardie: vertraging van de sinusale pace, normaal tijden rust en slaap,
intrinsieke of extrinsieke oorzaak, behandeling enkel nodig wanneer ↓CO
o Escape rhythm
Junctionaal: AV-knoop of proximale bundel van His, 40-60 bpm, nomale QRS
complexen zonder p-top
Ventriculair: 30-40 bpm, wijde QRS complexen
o AV-blok
Eerste graad: verlengde vertraging tussen atrium en ventrikel verlengd PR
interval, maar elke P top nog altijd gevolgd door een QRS complex, asymptomatisch
Tweede graad
Möbitz type I: P toppen op constante afstand, maar vertraging tussen
atrium en ventrikel wordt met elke slag groter totdat er een p-top niet
gevolgd wordt door een QRS complex en dan begint het opnieuw, meestal
asymptomatisch
-
Möbitz type II: geen progressieve verlenging van het PR interval maar
plotse blok waarbij gedurende een of enkele slagen een P top niet gevolgd
wordt door een QRS complex, ernstiger dan type I en pacemaker
aangewezen zelfs in asymptomatische patiënten
Derde graad: volledige disconnectie van de atria en ventrikels, P toppen volgen de
sinus knoop maar QRS complexen komen voort uit latente pacemaker cellen
Tachyaritmieën
o > 100 bpm ten minste 3 opeenvolgende slagen
o Supraventriculair
Sinustachycardie: 100-180 bpm, normale p toppen en QRS complexen
Atriale premature beats: eerder dan verwachte P top met abnormale vorm,
conductie geblokkeerd wanneer de p top zo snel op het vorige QRS complex volgt
dat het weefsel nog refractair is, enkel wanneer symptomatisch behandelen met βblokkers
Atriale flutter: 180-350 bpm, P toppen in de vorm van een zaag, niet 1 op 1 gevolgd
door QRS complex vanwege refractairiteit, meestal veroorzaakt door grote
gefixeerde reëntry-loop
Artiale fibrillatie: 350-600 bpm, P toppen zijn niet meer van elkaar te
onderscheiden, conductie naar ventrikels verloopt zeer onregelmatig ( ̴140-160
bpm), veroorzaakt door meerdere reëntry-loops
Paroxysmale supraventriculaire tachycardie: 140-250 bpm, plots begin en einde
AV knoop reëntry tachycardie (AVNRT): normale AV knoop heeft 2 of
meer pathways, soms zijn deze niet gelijk
o een pathway met snelle conductie en lange refractaire periode
o een pathway met trage conductie en korte refractaire priode
33
Atrioventriculaire reëntry tachycardie (AVRT): naast AV-knoop ook een
accesoire pathway beschikbaar
o
Wolff-Parkinson-White syndroom: accesoire pathway heeft
snellere conductie (kort PR interval en ‘slurred upstroke’ van QRS
oftewel delta wave)
Orthodrome reëntry: anterograad via AV knoop,
retrograad via accesoire pathway (retrograde P toppen)
Antidrome reëntry: anterograad via accesoire pathway,
retrograad via AV knoop (retrograde P toppen en wijd
QRS)
o Verborgen accesoire pathway: zoals orthodrome reëntry
o
Focale atriale tachycardie: door automaticiteit in een atriale ectopische locus of
reëntry, abnormale P top morfologie
Multifocale atriale tachycardie: ten minste 3 verschillende P top morfologieën,
gemiddeld > 100 bpm, vaak i.c.m. ernstige pulmonaire ziekte of hypoxie
Ventriculair
Ventriculaire premature beats: ectopische ventriculaire focus vuurt af en toe met
een wijd QRS complex, kan op zichzelf geen kwaad
Ventriculaire tachycardie: >3 opeenvolgende VPB’s, 100-200 bpm, wijd QRS
Nonsustained: <30 seconden
Sustained: > 30 seconden, met ernstige gevolgen (syncope, pulmonair
oedeem, hartstilstand) of nood aan cardioversie of farmacotherapie
o
VT onderscheiden van SVT door wijd QRS (niet altijd correct),
MI/hartfalen in de voorgeschiedenis, geen effect van vagale
manoeuvres, AV dissociatie
Torsades de Pointes: polymorfische VT met variërende amplitude van de QRS
complexen, uitgelokt door lang QT interval, meestal zelf-limiterend maar risico op
progressie naar VF
Ventriculaire fibrillatie: levensbedreigend, geen gecoördineerde hartcontracties
meer aanwezig met wegvallen van de CO, defibrillatie enige optie
34
Hoofdstuk 13
Hypertension
-
-
Systemen betrokken bij bloeddruk regulatie
o Hart
o Bloedvaten
o Nier
o Hormonen
Essentiële hypertensie (90%)
o Uitsluitingsdiagnose
o Familialiteit wordt vermoed maar is niet aangetoond
o Associatie met ouderdom, obesitas, diabetes mellitus type 2 en insuline resistentie
-
Bij ouderen wordt vasculaire weerstand een belangrijkere factor dan CO en komt er
vaker geïsoleerde systolische hypertensie voor (diastolisch druk normaal)
Secundaire hypertensie (10%)
o Onderliggende oorzaak te verwachen bij
o
Exogene oorzaken
o
Orale anticonceptiva
Sympathicomimetica (denk aan over-the-counter verkoudheidsmiddelen)
NSAID
Alcoholisme
Cocaïne
Renale oorzaken
o
Leeftijd <20 jaar of >50 jaar
Dramatisch gestegen bloeddruk
Abrupt begin
Geassocieerde symptomen
Negatieve familie geschiedenis
Renale parenchymale ziekte ↑intravasculaire volume / ↑renine
Arteria renalis stenose (atheroslerose of fibromusculaire dysplasie) ↑renine
Behandelen met PCI of heelkundige vaatreconstructie (ACE inhibitors enkel bij
unilaterale stenose)
Mechanische oorzaken
Coarctatie van de aorta (vernauwing ter hoogte van of juist distaal van de
aftakking van de a. subclavia sinistra)
o
Verminderde renale perfusie RAAS
Hogere druk poximaal van de vernauwing atherosclerose van arcus
aortae desensitisatie van de baroreceptoren
Behandelen met angioplastie/heelkunde (desensitisatie van baroreceptoren
blijft aanwezig)
Endocriene oorzaken
Feochromocytoom: catecholamine secreterende tumor van bijniermerg
Bijnierschors hormoon overmaat
Mineralocorticoiden (aldosteron): door bijnieradenoom of bilaterale
hyperplasie van de bijnieren of renine secreterende tumoren via RAAS,
natrium retentie met hypokaliëmie
35
Glucocorticoiden (cortisol) / Cushing: door ACTH secreterende tumor of
cortisol secreterend bijnieradenoom, bloedvolume expansie en stimulatie
van de synthese van RAAS componenten
Thyroidhormoon afwijkingen
o
o
-
Consequenties van hypertensie
o Vaak asymptomatisch, mogelijk flushing, zweten en wazig zicht
o Hart
o
o
Nefrosclerose hyalien infiltraat in de vaatwanden, gladde spiercel hypertrofie en
necrose in de capillairwanden ↓verminderde bloedtoevoer ischemische atrofie
van de tubules en glomeruli
Nierinsufficiëntie houdt chronische hypertensie in stand
Retina
Bloeding, exsudaat, locale infarctie vd retina of papil oedeem (acute hypertensie)
Arteriele vascoconstrictie, mediale hypertrofie tot sclerose (chronische hypertensie)
Meestal asymptomatische indicatoren voor de ernst en duur van de hypertensie,
soms aantasting van het zicht
Hypertensieve crisis
o
o
o
-
↑atherosclerose, aneurysmavorming, risico aortadissectie
Nieren
o
Hoog CVA risico (vooral afhankelijk van hoge systolische druk)
Hersenbloeding: scheuren van microaneurysmata
Herseninfarct: trombo-embolisatie vanuit carotiden
Aorta en perifere vasculatuur
o
↑afterload ↑wandspanning ventrikelhypertrofie
Stijf ventrikel diastolische dysfunctie pulmonaire congestie
Na enige tijd ook systolische dysfunctie ↓CO
↑coronaire atherosclerose en systolische workload risico myocard ischemie en
infarctie
Cerebrovasculair systeem
-
Hyperthyroidie: cardiale hyperreactiviteit + ↑ bloedvolume
Hypothyroidie: ↑perifere vasculaire weerstand
Verhoogde intracraniale druk encefalopathie hoofdpijn, wazig zicht, verwarring,
slaperigheid, soms coma
Retinale afwijkingen zoals hiervoor beschreven
Angina en pulmonair oedeem vanwege verhoogde hartarbeid
Behandeling
o Lifestyle aanpassingen
o Farmacologisch
Diuretica (thiazide)
Sympatholytica: β-blokkers: ↓HR en contractiliteit
Vasodilatoren: Calcium kanaal blokkers: ↓contractiilteit en perifere
vaatweerstand
Producten die interfereren met RAAS
ACE inhibitoren: ↓perifere vaatweerstand en natrium retentie,
↑bradykinine, nefroprotectief (droge hoest als neveneffect)
Angiotensine II receptor blokkers: vasodilatatie en ↓aldosteron
Directe renine inhibitoren
36
Hoofdstuk 14
Diseases of the pericardium
-
-
Acute pericarditis
o Oorzaak
Idiopatisch (meestal viraal maar dit wordt in klinische setting niet bewezen)
TBC bij immunogecompromiteerden
Bacterieel bij immunogecompromiteerden
Volgend op myocard infarct
Uremische pericarditis bij chronisch nierfalen
Neoplastische pericarditis
Radiatie geïnduceerde pericarditis
Geassocieerd met bindweefsel ziekten
Medicatie geïnduceerde pericarditis
o Inflammatoir proces: vasodilatatie met transsudaat verhoogde vasculaire
permeabiliteit leukocyten exsudaat
o De leukocyten vallen het infecterende of autoimmune agens aan, maar zorgen ook
voor een immuunrespons die schade en somatische symptomen zoals koorts geeft
o Pathofysiologie
Sereuze pericarditis: weinig witte bloedcellen in een dun waterig exsudaat,
waarschijnlijk vroege fase gelijk voor allee types acute pericarditis
Serofibrineuze pericarditis: exsudaat bevat plasma proteïnen, visceraal en
parietaal pericard kunnen verdikken en zelfs fuseren littekenweefsel
Purulente pericarditis: intense inflammatoire respons op bacteriële infectie
Hemorrhagische pericarditis: meestal veroorzaakt door TBC of maligniteit
o Symptomen en klinische tekens
Pijn op de borst: scherp, verergert met inspiratie of hoesten (pleuritis pijn)
en afhankelijk van positie
Koorts
Dyspneu
Wrijvingsgeruis
o Behandeling
Vaak zelf limiterend
1-3 weken rust
Pijnstilling (NSAID)
Colchicine vermindert recidief
Orale corticosteroïden enkel bij gecompliceerde gevallen
Katheter drainage en intensieve antibiotica bij purulente pericarditis
Uremische pericarditis dialyse
Neoplastische pericarditis palliatief
Pericardiale effusie
o >50 ml pericardiaal vocht
o Gevolg van acute pericarditis of niet-inflammatoire effusie door verhoogde capillaire
permeabiliteit, verhoogde capillaire hydrostatische druk of verminderde plasma
oncotische druk
37
o
-
-
Bij lage volumes blijft de intrapericardiale druk nagenoeg gelijk, maar boven een
bepaald punt zal een kleine volume vergroting een sterke druk verhoging tot gevolg
hebben (weinig compliantie)
o Symptomen en klinische tekenen
Asymptomatisch
Doffe pijn op de borst
Harttamponade
Dysfagie (compressie van de oesofagus)
Dyspneu (longcompressie)
Heesheid (compressie van n. laryngea recurrens)
Hik (stimulatie van de n. frenicus)
Gedempte harttonen
o Meest esensitieve diagnotische test is echocadiografie
o Behandeling
Onderliggende oorzaak behandelen
Pericardiocentesis bij groot volume en symptomen
Harttamponade
o De intrapericardiale druk is zo hoog dat er door compressie van de hartkamers een
sterke afname in SV en CO ontstaat met hypotensieve shock en dood als gevolg
o Oorzaak
Acute pericarditis
Bloeding door stomp of penetrerend thorax trauma
Bloeding door linker ventrikelwand ruptuur na MI
Bloeding door een gescheurd aneurysma van de aorta
o Symptomen en klinische tekenen
Diastolische druk wordt gelijk aan de pericardiale druk
Diastolisch vulling verzwakt
Pulmonaire en systemische congestie
↓SV ↓CO hypotensie en reflex tachycardie
Inadequate perfusie van vitale organen shock
Pulsus paradoxus: >10 mmHg vermindering in systolische bloeddruk bij
inademing
o Diagnose bij cardiale katheterisatie met therapeutische pericardiocentese
o Bij recurrente tamponade chirurgisch verwijderen van (een deel van) het pericard
Constrictieve pericarditis
o Gevolg van doorgemaakte pericarditis of TBC
o Pericardiale effusie wordt niet normaal geresorbeerd maar organiseert zich met fusie
van de pericardiale lagen en littekenvorming als gevolg, mogelijk zelfs calcificatie
o Diastolische dysfunctie
o Symptomen en klinische tekenen
↓SV en CO hypotensie met reflex tachycardie
Systemische congestie (rechterhartfalen)
Kussmaul teken: jugulaire venen meer opgezet tijdens inspiratie
o Behandeling: chirurgisch verwijderen van het pericard
38
Hoofdstuk 16
Congenital heart disease
-
-
Foetale circulatie (sluit normaal zodra de longen beginnen te werken na de geboorte)
o Ductus venosus: shunt bloed van de v. umbilicus rechtstreeks naar de vena cava
inferior (buiten de portale circlatie om)
o Foramen ovale: opening tussen atria die goed geoxygeneerd bloed uit de VCI van het
rechter naar het linker atrium shunt (aangezien er nog geen oxygenatie gebeurt in de
foetale longen)
o Ductus arteriosus: verbinding tussen truncus pulmonalis en aortaboog zodat de
longen voor een groot deel gebypassed worden
Acyanotische defecten
o Atriaal septum defect
Verbinding tussen de atria door schade van het atriale septum (sinus
venosus defect en patent foramen ovale zijn hier technisch gezien niet aan
gelijk, maar presenteren wel hetzelfde)
Left-to-right shunt volume overload en dilatatie van het rechter atrium en
ventrikel
Afname van rechter ventrikel compliantie kan shunting verminderen
Meestal asymptomatisch, anders inspanningsdyspneu, moeheid en
terugkerende lage luchtweg infecties, atriale tachycardie op latere leeftijd
o Ventriculaire septum defect
Left-to-right shunt volume overload van rechter ventrikel, pulmonaire
circulatie en linker atrium en –ventrikel
Initieel ↑SV, later systolische dysfunctie en hartfalen
Soms spontaan herstel, anders chirurgische correctie in kinderleeftijd
o Patente ductus arteriosus
Shunt van aort richting linker a. pulmonalis door druk gradiënt volume
overload van pulmonaire circulatie, linker atrium en –ventrikel (linker
hartfalen)
Spontaan sluiten kan in de eerste maanden van het leven, anders medicinaal
sluiten d.m.v. prostaglandineinhibitors, heelkundig sluiten of
transkatheterisatie met coiling
o Congenitale aorta stenose
Meestal veroorzaakt door bicuspiede aortaklep, veroorzaakt soms pas
stenose na vele jaren
↑systolische linker ventriculaire druk hypertrofie
Risico aorta aneurysma
Behandeling meestal niet noodzakelijk, anders ballon valvuloplastie of
heelkundig ingrijpen
o Pulmonale stenose
Obstructie t.h.v. pulmonaalklep, a. pulmonalie of in het outflowtraject van
de rechter ventrikel
↑systolische rechter ventriculaire druk hypertrofie
Kan leiden tot rechter hartfalen
39
-
-
Behandeling meestal niet noodzakelijk, anders ballon valvuloplastie
o Aorta coarctatie
Vaak geassocieerd met bicuspiede aortaklep
↑ afterload met beperkte flow naar onderlichaam
Meestal asymptomatisch, soms claudicatio klachten en hypertensie in de
bovenste lichaamshelft
Bij jonge kinderen is heelkundige correctie aangewezen, bij oudere kinderen
en volwassenen kunnen transkatherer interventies voldoen
Cyanotische defece
o Tetralogy van Fallot
4 anomaliën
Subvalvulaire pulmonale stenose
Rechterventrikel hypertrofie
Ventrikel septum defect
Aorta ontvangt bloed uit beide ventrikels
Als gevolg wordt zuurstof arm bloed uit de systemische circulatie
rechtstreeks teruggepompt in de aorta, de longen worden geshunt
Inspanning,eten of huilen kan leiden tot verhoogde right-to-left shunt met
prikkelbaarheid, cyanose, hyperventilatie en evt. syncope of convulsies
Chronische hypoxemie kan leiden tot clubbing van vingers en tenen
Behandeling is heelkundig sluiten van het VSD en vergroten van het
pulmonaire outflowtraject
o Transpositie van de grote arteriën
Aorta ontsrpingt aan het rechterventrikel en truncus pulmonalis aan het
linker ventrikel
Systemische circulatie is nu parallel geschakeld aan de pulmonaire circulatie
en er vindt dus geen oxygenatie van sysemisch bloed plaats fataal
Toedienen van prostaglandinen houdt de ductus arteriosus open en het
foramen ovale kan opn gehouden worden door ballonkatheterisatie zodat er
menging kan zijn van de twee systemen
Definitieve correctie is heelkundig verwisselen van de aorta en truncus
pulmonalis tot de natuurlijke positie
Eisenmenger syndroom
o Bij ernstig pulmonair vasculair lijden door chronische left-to-right shunt, kan de flow
omdraaien right-to-left shunt hypoxemie en cyanose
o Symptomen
Inspanningsdyspneu en moeheid
Erythrocytose
Hyperviscositeit
Moeheid
Hoofdpijn
CVA
Clubbing van de vingers
o Enkel palliatieve behandeling of hart-long transplantatie mogelijk
40