12
13
14
15
16
17
18
19
20
Ho YV, Frauman AG, Thomson W, Seeman E. Effects of alendronate on bone density in men with primary and secondary osteoporosis. Osteoporos Int 2000;11:98-101.
Schuit SCE, Klift M van der, Weel AEAM, Laet CEDH de, Burger
H, Seeman E, et al. Fracture incidence and association with bone
mineral density in elderly men and women: the Rotterdam study.
Bone 2004;34:195-202.
World Health Organization. Assessment of fracture risk and its
application to screening for postmenopausal osteoporosis. Report of
a WHO Study Group. World Health Organ Tech Rep Ser 1994;
843:1-129.
Kanis JA. Assessment of fracture risk and its application to screening for postmenopausal osteoporosis: synopsis of a WHO report.
WHO Study Group. Osteoporos Int 1994;4:368-81.
Genant HK, Wu CY, Kuijk C van, Nevitt MC. Vertebral fracture
assessment using a semiquantitative technique. J Bone Miner Res
1993;8:1137-48.
Eastell R, Barton I, Hannon RA, Chines A, Garnero P, Delmas PD.
Relationship of early changes in bone resorption to the reduction in
fracture risk with risedronate. J Bone Miner Res 2003;18:1051-6.
Sambrook PN, Geusens P, Ribot C, Solimano JA, FerrierBarriendos J, Gaines K, et al. Alendronate produces greater effects
than raloxifene on bone density and bone turnover in postmenopausal women with low bone density: results of EFFECT (Efficacy
of FOSAMAX versus EVISTA comparison trial) international.
J Intern Med 2004:255:503-11.
Freedman KB, Kaplan FS, Bilker WB, Strom BL, Lowe RA.
Treatment of osteoporosis: are physicians missing an opportunity?
J Bone Joint Surg Am 2000;82-A:1063-70.
Panneman MJM, Lips P, Sen SS, Herings RMC. Undertreatment
with anti-osteoporotic drugs after hospitalization for fracture.
Osteoporos Int 2004;15:120-4.
21
22
23
24
25
26
27
28
Cummings SR, Black DM, Nevitt MC, Browner W, Cauley J,
Ensrud K, et al. Bone density at various sites for prediction of hip
fractures. The Study of Osteoporotic Fractures Research Group.
Lancet 1993;341:72-5.
Seeman E, Eisman JA. Treatment of osteoporosis: why, whom,
when and how to treat. The single most important consideration is
the individual’s absolute risk of fracture. Med J Aust 2004;180:
298-303.
Marshall D, Johnell O, Wedel H. Meta-analysis of how well
measures of bone mineral density predict occurrence of osteoporotic fractures. BMJ 1996;312:1254-9.
Silverman SL, Minshall ME, Shen W, Harper KD, Xie S. The relationship of health-related quality of life to prevalent and incident
vertebral fractures in postmenopausal women with osteoporosis:
results from the Multiple outcomes of raloxifene evaluation study.
Health-Related Quality of Life Subgroup of the Multiple outcomes
of raloxifene evaluation study. Arthritis Rheum 2001;44:2611-9.
Nevitt MC, Ettinger B, Black DM, Stone K, Jamal SA, Ensrud K, et
al. The association of radiographically detected vertebral fractures
with back pain and function: a prospective study. Ann Intern Med
1998;128:793-800.
Ismail AA, Cockerill W, Cooper C, Finn JD, Abendroth K, Parisi
G, et al. Prevalent vertebral deformity predicts incident hip though
not distal forearm fracture: results from the European prospective
osteoporosis study. Osteoporos Int 2001;12:85-90.
Dhesi JK, Moniz C, Close JCT, Jackson SHD, Allain TJ. A rationale for vitamin D prescribing in a falls clinic population. Age Ageing
2002;31:267-71.
Fisher A, Davis M. Is there rationale for vitamin D prescribing in
the elderly population? Age Ageing 2003;32:235-6.
Aanvaard op 21 april 2004
Casuïstische mededelingen
Deficiëntie van het vetzuuroxidatie-enzym
middenketen-acyl-coënzym-A-dehydrogenase (MCAD) bij een volwassene,
opgespoord tijdens een proefproject voor neonatale screening
t.g.j.derks, h.jakobs, a.gerding, k.e.niezen-koning, d-j.reijngoud en g.p.a.smit
De meest voorkomende erfelijke metabole ziekte in de
verbranding van vetzuren is deficiëntie van het enzym
middenketen-acyl-coënzym-A-dehydrogenase (MCAD;
enzymnummer: EC 1.3.99.3); de ziekte heeft als identificatiecode in de ‘online Mendelian inheritance in man’
(OMIM; www.ncbi.nlm.nih.gov/entrez/dispomim.cgi?id
=201450): 201450.1
In dit artikel beschrijven wij een Nederlandse familie
waarin de ziekte voorkomt en waarvan de ziektegeschiedenis van de oudste twee kinderen in 1965 reeds
in dit tijdschrift werd bediscussieerd.2
Academisch Ziekenhuis, Beatrix Kinderkliniek, Postbus 30.001, 9700
RB Groningen.
Sectie Metabole Ziekten: hr.T.G.J.Derks, arts-onderzoeker; hr.dr.
G.P.A.Smit, kinderarts metabole ziekten.
Laboratorium Metabole Ziekten: hr.A.Gerding, analist; mw.dr.K.E.
Niezen-Koning, klinisch biochemisch geneticus; hr.dr.D-J.Reijngoud,
klinisch chemicus.
Hr.H.Jakobs, huisarts te Leeuwarden.
Correspondentieadres: hr.T.G.J.Derks ([email protected]).
Samenvatting: zie volgende bladzijde.
de ziekte mcad-deficiëntie
Biochemie. MCAD is het enzym dat verantwoordelijk is
voor de eerste stap in de β-oxidatie van de middenketenvetzuren in mitochondria. Personen met deze
aandoening kunnen lange-ketenvetzuren slechts tot
vetzuren met middellange keten verbranden. Als gevolg
hiervan worden vetzuren in beperkte mate geoxideerd,
waardoor de synthese van ketonlichamen beperkt
is. Hierdoor kan bij jonge kinderen met deze aandoening een periode van verminderde voedselinname of
verhoogde energiebehoefte, bijvoorbeeld als reactie op
een eenvoudige infectie, leiden tot een metabole ontsporing waarbij een hypoketotische hypoglykemie optreedt.3 4
Kliniek. De belangrijkste klinische verschijnselen die
vervolgens kunnen optreden, zijn lethargie, braken, coNed Tijdschr Geneeskd 2004 30 oktober;148(44)
2185
samenvatting
Sinds oktober 2003 wordt in de provincies Friesland, Groningen, Drenthe en Overijssel doelmatigheidsonderzoek uitgevoerd waarbij pasgeborenen worden gescreend op deficiëntie
van middenketen-acyl-coënzym-A-dehydrogenase (MCAD)
in aanvulling op het reguliere hielprikonderzoek op fenylketonurie, congenitale hypothyreoïdie en adrenogenitaal syndroom. Een van de vragen in dit onderzoek betreft de oorzaak
van de sterk variërende klinische expressie van dit ziektebeeld.
Hierbij is onderdiagnostiek een belangrijk element, zoals blijkt
uit de gegevens van een familie waarvan de ziektegeschiedenis
van de oudste 2 kinderen in 1965 in dit tijdschrift werd bediscussieerd. Beide kinderen overleden op zeer jonge leeftijd.
Recent werd de diagnose ‘MCAD-deficiëntie’ gesteld bij het
jongste kind uit hetzelfde gezin, inmiddels een 34-jarige vrouw.
Deze familieanamnese illustreert de variabele klinische expressie van het ziektebeeld, dat gepaard kan gaan met sterfte,
maar dat bij andere kinderen ook zeer licht en subklinisch kan
verlopen. Tevens illustreert deze familieanamnese dat ook onderdiagnostiek bij overleden kinderen een oorzaak kan zijn
van een ogenschijnlijk beperkte klinische detectiegraad van
deze aandoening, die na het stellen van de diagnose uitstekend
behandelbaar is door leefstijl- en dieetmaatregelen.
ma, convulsies en soms kan de patiënt zelfs overlijden.
De overmaat van middenketenvetzuren wordt langs een
alternatieve metabole route omgezet in dicarbonzuren,
glycineconjugaten en acylcarnitinen van corresponderende ketenlengte en in de urine uitgescheiden (figuur 1).
Analyse van de organische zuren door middel van
gaschromatografie-massaspectrometrie in de nuchtere
ochtendurine maakt het mogelijk deze metabolieten te
detecteren en te identificeren. De diagnose ‘MCADdeficiëntie’ wordt bevestigd door meting van de enzymactiviteit in leukocyten of fibroblasten.
Erfelijkheid. Ongeveer 80% van de patiënten met een
klinisch manifest ziektebeeld is homozygoot voor de
985GA-puntmutatie in het MCAD-gen, dat gelokaliseerd is op de korte arm van chromosoom 1.5 De overerving is autosomaal recessief.
Beloop en behandeling. Hoewel een metabole ontsporing ten gevolge van MCAD-deficiëntie met ernstige
morbiditeit en sterfte gepaard kan gaan, is het beloop
doorgaans ongecompliceerd na het stellen van de diagnose en het instellen van leefstijl- en dieetmaatregelen.6
Onder normale omstandigheden dienen kinderen met
MCAD-deficiëntie iedere vorm van vasten te vermijden.
De behandeling bestaat daarom uit frequente koolhydraatverrijkte maaltijden, waardoor jonge kinderen
nog een late avondvoeding krijgen. Een aantal kinderen
lijkt minder vaak en minder snel metabool te ontsporen
wanneer riboflavine en/of carnitine wordt gebruikt.1 3
Riboflavine is de precursor van flavine-adenine-dinucleotide (FAD), dat als cofactor van het MCAD-enzym
dient. Carnitine kan worden gebruikt ter bevordering
van de excretie van acylcarnitinen. De behandeling in
stresssituaties (waarin vaak een combinatie van koorts,
braken, diarree en voedselweigering optreedt) bestaat
uit dezelfde elementen, waarbij een laagdrempelig contact met de tweede lijn erg belangrijk is indien de orale
2186
Ned Tijdschr Geneeskd 2004 30 oktober;148(44)
inname van glucosebevattende producten niet gewaarborgd kan worden.5
Bevolkingsonderzoek. Sinds enkele jaren is er een
nieuwe analysemethode beschikbaar die het mogelijk
maakt in plasma vetzuuroxidatiedefecten zoals MCADdeficiëntie te diagnosticeren, onafhankelijk van de
klinische verschijnselen. Bij deze methode meet men
acylcarnitinen, tussenproducten in de vetzuuroxidatie.
Hiervoor kan men gebruikmaken van een bloedvlek,
verkregen uit een hielprik. De meting geschiedt met zogenaamde tandem-massaspectrometrie. In de afgelopen
jaren werd deze methode van opsporing reeds toegepast in het bevolkingsonderzoek van pasgeborenen in
delen van de VS, Canada, Duitsland en Australië.7 In
Nederland worden pasgeborenen momenteel gescreend
op fenylketonurie, congenitale hypothyreoïdie en het
adrenogenitaal syndroom. Vanaf oktober 2003 worden
pasgeborenen in de provincies Friesland, Groningen,
Drenthe en Overijssel in aanvulling op het landelijke
hielprikprogramma gescreend op MCAD-deficiëntie. In
diverse regionale en landelijke media is aandacht geweest voor dit aanvullende hielprikprogramma, dat het
karakter heeft van een doelmatigheidsonderzoek.
De betrokken familie. Naar aanleiding van een publicatie over dit onderzoek in een regionaal dagblad en de
mitochondriële
β-oxidatie
ω-oxidatie
verzadigd
langketen-acyl-CoA
ω-1-oxidatie
dodecaanzuur
dodecanoyl-CoA
11-OH-dodecaanzuur
sebacinezuur
decanoyl-CoA
9-OH-decaanzuur
suberinezuur
octanoyl-CoA
7-OH-octaanzuur
adipinezuur
hexanoyl-CoA
5-OH-hexaanzuur
suberylglycine
butyryl-CoA
octanoylcarnitine
hexanoylglycine
acetyl-CoA
hexanoylcarnitine
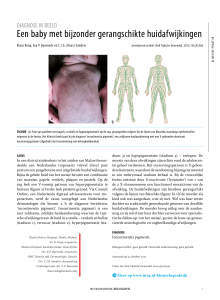
figuur 1. Vereenvoudigde weergave van alternatieve metabole routes van acylcoënzym-A(CoA)-esters bij deficiëntie van
het middenketen-acyl-CoA-dehydrogenase (MCAD) waarbij
langeketenvetzuren slechts tot vetzuren van middellange keten
verbrand kunnen worden. Bij normale vetzuurverbranding
worden vrije vetzuren aan CoA gekoppeld. Vervolgens ondergaan deze acyl-CoA-esters β-oxidatie, een cyclisch proces. Bij
iedere cyclus die is samengesteld uit 4 opeenvolgende reacties,
vindt afsplitsing plaats van de laatste 2 koolstofatomen onder
vorming van acetyl-CoA. Acetyl-CoA is essentieel in de ketogenese. Het MCAD-enzym is betrokken bij de eerste stap
van de mitochondriële β-oxidatie van middenketen-acyl-CoAesters. In de figuur wordt met de rode balken het enzymdefect
bij MCAD-deficiëntie gesymboliseerd. De middenketenacyl-CoA-esters die niet normaal verwerkt kunnen worden ondergaan alternatieve oxidatie in peroxisomen en microsomen.
Bij deze ω- en ω-1-oxidatie wordt respectievelijk het laatste of
het één na laatste koolstofatoom betrokken. Dit leidt tot de
vorming van metabolieten, die pathognomonisch zijn voor
MCAD-deficiëntie. Deze metabolieten zijn aantoonbaar in
crisissituaties, maar zijn ook te vinden in nuchtere ochtendurine (vet aangegeven) en plasma (vet en cursief).
recente geboorte van haar derde kind nam een 34-jarige
vrouw (patiënt C; zie verder) in samenspraak met haar
huisarts contact op met onze afdeling. In de summiere
beschrijving van het ziektebeeld in de publicatie herkenden beiden gebeurtenissen binnen de familie van de
vrouw. In dit artikel beschrijven wij haar anamnese en
de familieanamnese en bespreken wij hoe uiteindelijk
bij deze vrouw de diagnose ‘MCAD-deficiëntie’ werd
gesteld. De ziektegeschiedenissen van haar oudere zus
en broer (patiënt A en B; zie verder) werden reeds in
1965 in dit tijdschrift besproken in een ingezonden
brief.2 Destijds werden onder andere een intoxicatie en
het Reye-syndroom als differentiaaldiagnostische mogelijkheden besproken. De familieanamnese illustreerde
enkele aspecten van de diversiteit in klinische expressie
van het ziektebeeld, dat gepaard kan gaan met sterfte,
maar bij andere patiënten ook beduidend lichter kan
verlopen. In dit artikel schenken wij aan de hand van
deze familieanamnese aandacht aan de klinische variabiliteit van MCAD-deficiëntie, de epidemiologische gegevens en de implicaties voor dit bevolkingsonderzoek
bij pasgeborenen.
ziektegeschiedenissen
Patiënt A was een dochter van niet-consanguïene ouders, die
zich na een niet-afwijkende zwangerschap en partus in de jaren
zestig van de vorige eeuw aanvankelijk normaal had ontwikkeld.2 De voorgeschiedenis vermeldde een ‘koortsstuip’ op de
leeftijd van 11 maanden bij otitis media dextra en angina. Toen
zij 16 maanden oud was, werd patiënte ziek met verschijnselen
van acute gastro-enteritis en lichte temperatuurverhoging. Na
2 dagen werd zij ’s ochtends stuipend, apathisch en slap in bed
aangetroffen en zij werd in comateuze toestand in het ziekenhuis opgenomen. Het laboratoriumonderzoek bij opname liet
een bloedsuikerconcentratie van 5,5 mmol/l zien en de urine
vertoonde een zwakke reactie op aceton. Ondanks behandeling met anti-epileptica kreeg patiënte convulsies en het beloop
werd gecompliceerd door melaena, waarbij zij in shock raakte.
Zij werd geopereerd, waarbij een sterk vergrote vaste bleekgele lever werd gezien; 12 h later overleed zij. Bij de obductie
werd het bestaan van een sterk vergrote botergele lever bevestigd, microscopisch bestond er parenchymateuze vervetting
van lever, nieren en myocard.
Patiënt B, een jongetje, zoals gezegd het broertje van patiënt
A, werd geboren na een ongestoorde zwangerschap en partus.2
Na de geboorte werd patiënt gehongerd om het geven van
borstvoeding te bevorderen; hij kreeg geen bijvoeding. Ongeveer 24 h na de geboorte werd opgemerkt dat het kind wat kort
ademde. Vier uur later overleed hij plotseling en bij obductie
viel een wat gevlekte lever op. Microscopisch onderzoek van
lever, hart, nieren en skeletspier liet eenzelfde vettige degeneratie zien als bij patiënt A. In de hersenen werd oedeem gevonden in schors en merg.
Patiënt C werd als vierde kind en tweede dochter in hetzelfde
gezin geboren en ontwikkelde zich voorspoedig na een normale zwangerschap en partus. Op de leeftijd van 16 maanden werd
zij ’s ochtends comateus in bed aangetroffen. De dagen ervoor
had zij minder gegeten en gedronken bij een gastro-enteritis en
koorts. Bij opname in het ziekenhuis ging het om een hypotoon, comateus meisje met een hepatomegalie. De glucoseconcentratie in het bloed was onmeetbaar laag en 5 min na een
intraveneuze bolusinjectie van glucose begon patiënte weer te
reageren. Gedurende de opname trad er nog enkele malen een
hypoglykemie op, vooral indien haar enige tijd geen voedsel
gegeven was. Bij het ontslag werd aan de ouders geadviseerd
haar een late avondvoeding te geven en vasten tijdens infecties
te vermijden. Vervolgens deden zich gedurende haar jeugd en
ook daarna geen nieuwe voorvallen voor.
Patiënte werd, zoals reeds vermeld, op 34-jarige leeftijd verwezen naar onze polikliniek voor metabole ziekten. Er werd
oriënterend metabool onderzoek verricht met als differentiaaldiagnose ‘vetzuuroxidatiestoornis’. Analyse van de organische
zuren in nuchtere ochtendurine liet uitscheiding zien van metabolieten die kenmerkend zijn voor MCAD-deficiëntie (figuur 2).
In het plasma waren de concentraties van hexanoylcarnitine,
octanoylcarnitine, decenoylcarnitine en decanoylcarnitine verhoogd. De MCAD-enzymactiviteit gemeten in leukocyten van
patiënte werd deficiënt bevonden. Zoals te doen gebruikelijk
werd vervolgens MCAD-mutatieonderzoek ingezet en werd
het onderzoek van familieleden gestart.
beschouwing
Algemeen wordt aangenomen dat de eerste klinische
beschrijving van een patiënt met MCAD-deficiëntie dateert uit 1976.8 Doordat bijna 40 jaar na dato bij patiënt
C de diagnose ‘MCAD-deficiëntie’ kon worden gesteld,
bleek dat de ingezonden brief in dit tijdschrift in 1965
waarin patiënt A en B werden beschreven waarschijnlijk
de oudste bekende (Nederlandstalige) referentie is van
jonge kinderen met deze aandoening. Deze oorspronkelijke publicatie bevat een nauwkeurige beschrijving van
het klinische verloop van een metabole ontsporing ten
gevolge van MCAD-deficiëntie, waarbij het optreden
van een hypoketotische hypoglykemie pathognomonisch genoemd kan worden. Bovendien illustreert de
familiegeschiedenis een aantal relevante zaken voor
criteria voor bevolkingsonderzoek van pasgeborenen
op deze aandoening: de sterfte door en prevalentie van
MCAD-deficiëntie.
Sterfte door MCAD-deficiëntie. Volgens overzichtsartikelen waarin cohorten van patiënten met MCADdeficiëntie worden beschreven, overlijdt bijna 20% van
de kinderen als gevolg van een metabole ontsporing nog
voordat de diagnose gesteld kan worden.3 9 Daarentegen
zijn sterfte en morbiditeit na het stellen van de diagnose
ongebruikelijk.6
Al in 1984 verscheen de eerste publicatie waarin de
relatie tussen wiegendood (‘sudden infant death syndrome’; SIDS) en MCAD-deficiëntie werd beschreven.10 Vervolgens werd retrospectief in diverse publicaties beschreven wat het aandeel is van patiënten met
MCAD-deficiëntie in een populatie overleden kinderen
bij wie het overlijden was gekarakteriseerd als ‘SIDS’ of
als ‘plotse onverwachte dood op zuigelingenleeftijd’
(‘sudden unexpected death in infancy’; SUDI). Aan
de hand van 985GA-mutatiedetectie in postmortaal
materiaal van 1236 SIDS-kinderen werd bepaald dat
MCAD-deficiëntie hierin geen belangrijke rol speelt.11
Na analyse van postmortaal leverweefsel van 418 casussen van SUDI werd geconcludeerd dat er bij 5% een vetzuuroxidatiestoornis was.12 Anderen pasten tandemmassaspectrometrie toe om acylcarnitinen in plasma te
bepalen van 7058 kinderen met SIDS.13 Zij identificeerden 23 kinderen met MCAD-deficiëntie (0,3%).
Ned Tijdschr Geneeskd 2004 30 oktober;148(44)
2187
1
100
5 6
10
3
relatieve hoeveelheid
80
2
60
40
8
20
7
0
10
20
30
40
50
tijd (in min)
10
12
a
9
6
100
8
relatieve hoeveelheid
80
5
60
7
40
4
3
1
20
2
11
0
b
10
20
30
40
50
tijd (in min)
figuur 2. Analyse van de organische zuren door middel van gaschromatografie-massaspectrometrie in de urine van een gezond
kind na vasten (a), vergeleken met nuchtere ochtendurine van patiënt C (b); bij patiënt C werden de metabolieten aangetroffen
die kenmerkend zijn voor deficiëntie van middenketen-acyl-coënzym-A-dehydrogenase (MCAD) en die als volgt zijn genummerd: 1 = β-hydroxyboterzuur; 2 en 3 = acetoacetaat; 4 = 5-hydroxyhexaanzuur; 5 = adipinezuur; 6 = 4-fenylboterzuur (interne
standaard); 7 = onverzadigd suberinezuur; 8 = suberinezuur; 9 = hexanoylglycine; 10 = C17:0-vetzuur (interne standaard); 11 =
fenylpropionylglycine; 12 = suberylglycine. De piekhoogten zijn uitgedrukt als percentages ten opzichte van de interne standaard
4-fenylboterzuur.
De retrospectieve opzet van deze studies impliceert
een selectie van kinderen bij wie na overlijden postmortaal onderzoek is verricht. Bovendien werden veelal kinderen geïncludeerd met een leeftijd van 1 week tot
1 jaar. Van MCAD-deficiëntie is bekend dat bij deze
ziekte zowel op de neonatale leeftijd als op de latere
kleuterleeftijd sterfte en morbiditeit kunnen vóórkomen
indien de diagnose niet eerder gesteld is. Verder is informatie over de demografische gegevens van de onderzoeksgroep essentieel. Dit wordt geïllustreerd door de
SUDI-populatie, afkomstig uit Maryland (VS).12 Van
2188
Ned Tijdschr Geneeskd 2004 30 oktober;148(44)
deze kinderen was 50% van negroïde afkomst, terwijl de
985GA-MCAD-mutatie vooral vóórkomt onder blanken.14 Tenslotte zijn wij van mening dat analyse van het
aandeel van kinderen met MCAD-deficiëntie in een
populatie overleden kinderen niet beperkt zou moeten
worden tot SIDS of onverklaarbaar overlijden, omdat
kinderen met MCAD-deficiëntie vaak aan een bijkomende aandoening overlijden.
Prevalentie en penetrantie van MCAD-deficiëntie in
relatie tot neonatale screening. Op basis van het vóórkomen van de 985GA-mutatie is een schatting gemaakt
van de prevalentie van MCAD-deficiëntie in Nederland:
deze bedraagt 1:12.100 (95%-BI: 1:8450-1:18.500).15 Dit
betekent dat er in Nederland jaarlijks gemiddeld 16-17
kinderen met deze aandoening geboren worden en daarmee komt MCAD-deficiëntie vaker voor dan fenylketonurie.16 Algemeen wordt aangenomen dat het aantal
klinisch gediagnosticeerde casussen belangrijk minder is
dan het aantal dat voorspeld wordt op grond van de prevalentie van de 985GA-mutatie.17 Bovendien lijkt dit
verschil regionaal bepaald.18 In welke mate dit voor de
Nederlandse situatie geldt, is momenteel onderwerp van
een landelijke retrospectieve studie.
Het is bekend dat de variatie in klinische expressie
van het ziektebeeld groot is. Sommige patiënten presenteren zich buiten de klassieke leeftijdsperiode van 0,5-4
jaar, bijvoorbeeld als volwassene.19 20 Neonatale manifestatie van de ziekte komt ook voor, zelfs voordat de uitslag van een hielprikonderzoek beschikbaar kan zijn.21
Het is opvallend dat er sinds de opkomst van neonatale
screeningsprogramma’s voor MCAD-deficiëntie weinig
aandacht is besteed aan het aandeel patiënten met een
neonatale manifestatie. Bij een aantal patiënten blijft de
MCAD-deficiëntie ongediagnosticeerd tot de diagnose
bij broers of zussen wordt gesteld; dit geldt voor zowel
patiënten met subklinische ziekte als acuut overleden
kinderen.22
conclusie
MCAD-deficiëntie is een bekende oorzaak van acuut
overlijden van jonge kinderen. Desondanks wordt deze
diagnose niet altijd overwogen of uitgesloten bij overleden kinderen met verdachte klinische verschijnselen.
Hierdoor lopen overige kinderen binnen het gezin dezelfde risico’s, omdat het immers een erfelijke aandoening betreft. Wij wijzen erop dat er momenteel in een
deel van ons land een doelmatigheidsonderzoek plaatsvindt naar de haalbaarheid van neonatale screening voor
deze aandoening. De resultaten van dat onderzoek kunnen bijdragen aan een gunstiger klinisch beloop voor
patiënten met deze soms fatale aandoening. Immers,
indien de aandoening tijdig wordt herkend, kunnen
ernstige morbiditeit en sterfte worden voorkomen na
instellen van eenvoudige therapeutische maatregelen.
A.van Assen, T.Boer en A.Hammer-ter Harmsel droegen bij
aan de analyse van de gegevens. De direct betrokken familieleden van de patiënten gaven commentaar op de ziektegeschiedenissen.
to the regular newborn screening programme for phenylketonuria, congenital hypothyroidism and adrenogenital syndrome.
One of the questions to be answered by this trial is the cause
of the strong variation in clinical expression of the disorder.
Underdiagnosing is an important factor in this phenomenon, as
shown by the data of a family of which the case histories of the
two oldest children were discussed in this journal in 1965. Both
children died at a very young age. Recently, MCAD deficiency was diagnosed in the youngest child of this family, now a
34-year-old woman. This family history illustrates the variable
clinical expression of MCAD deficiency, which can cause death
but can also run a milder or even subclinical course. Moreover,
this family history shows that the underdiagnosis of MCAD deficiency in deceased children may be a cause of the apparently
limited clinical detection rate of this disease, for which a simple treatment consisting of life-style and dietary measures is
available after diagnosis.
1
2
3
4
5
6
7
8
9
10
11
12
Belangenconflict: geen gemeld. Financiële ondersteuning: de
pilotscreening op MCAD-deficiëntie in Noordoost-Nederland
wordt gefinancierd door ZonMw.
abstract
Deficiency of the fatty-acid oxidising enzyme medium-chain
acyl-CoA dehydrogenase (MCAD) in an adult, detected during
a neonatal screening programme. – In a trial running since
October 2003 in the Dutch provinces of Friesland, Groningen,
Drenthe and Overijssel neonatal screening for medium-chain
acyl-CoA dehydrogenase (MCAD) deficiency has been added
13
14
literatuur
Roe CR, Ding J. Mitochondrial fatty acid oxidation disorders. In:
Scriver CR, Beaudet AL, Sly WS, Valle D, editors. The metabolic &
molecular bases of inherited disease. New York: McGraw-Hill; 2001.
p. 2297-326.
Nolen W, Schoot HCM van der. Een kind met encephalitis [ingezonden]. Ned Tijdschr Geneeskd 1965;109:1398-400.
Iafolla AK, Thompson jr RJ, Roe CR. Medium-chain acyl-coenzyme A dehydrogenase deficiency: clinical course in 120 affected
children. J Pediatr 1994;124:409-15.
Houwen RHJ, Nelck GF, Reijngoud D-J, Grond J, Smit GPA,
Bijleveld CMA. Twee patiënten met het syndroom van Reye? Ned
Tijdschr Geneeskd 1988;132:2025-8.
Gregersen N, Blakemore AI, Winter V, Andresen B, Kolvraa S,
Bolund L, et al. Specific diagnosis of medium-chain acyl-CoA
dehydrogenase (MCAD) deficiency in dried blood spots by a polymerase chain reaction (PCR) assay detecting a point-mutation
(G985) in the MCAD gene. Clin Chim Acta 1991;203:23-34.
Wilson CJ, Champion MP, Collins JE, Clayton PT, Leonard JV.
Outcome of medium chain acyl-CoA dehydrogenase deficiency
after diagnosis. Arch Dis Child 1999;80:459-62.
Pandor A, Eastham J, Beverley C, Chilcott J, Paisley S. Clinical effectiveness and cost-effectiveness of neonatal screening for inborn
errors of metabolism using tandem mass spectrometry: a systematic
review. Health Technol Assess 2004;8:iii,1-121.
Gregersen N, Lauritzen R, Rasmussen K. Suberylglycine excretion
in the urine from a patient with dicarboxylic aciduria. Clin Chim
Acta 1976;70:417-25.
Pollitt RJ, Leonard JV. Prospective surveillance study of medium
chain acyl-CoA dehydrogenase deficiency in the UK. Arch Dis
Child 1998;79:116-9.
Howat AJ, Bennett MJ, Variend S, Shaw L. Deficiency of medium
chain fatty acylcoenzyme A dehydrogenase presenting as sudden
infant death syndrome. BMJ 1984;288:976.
Arens R, Gozal D, Jain K, Muscati S, Heuser ET, Williams JC, et al.
Prevalence of medium-cain acyl-coenzyme A dehydrogenase deficiency in the sudden infant death syndrome. J Pediatr 1993;122
(5 Pt 1):715-8.
Boles RG, Buck EA, Blitzer MG, Platt MS, Cowan TM, Martin SK,
et al. Retrospective biochemical screening of fatty acid oxidation
disorders in postmortem livers of 418 cases of sudden death in the
first year of life. J Pediatr 1998;132:924-33.
Chace DH, DiPerna JC, Mitchell BL, Sgroi B, Hofman LF, Naylor
EW. Electrospray tandem mass spectrometry for analysis of acylcarnitines in dried postmortem blood specimens collected at autopsy from infants with unexplained cause of death. Clin Chem 2001;
47:1166-82.
Tanaka K, Gregersen N, Ribes A, Kim J, Kolvraa S, Winter V, et al.
A survey of the newborn populations in Belgium, Germany, Poland,
Czech Republic, Hungary, Bulgaria, Spain, Turkey, and Japan for
the G985 variant allele with haplotype analysis at the medium chain
acyl-CoA dehydrogenase gene locus: clinical and evolutionary consideration. Pediatr Res 1997;41:201-9.
Ned Tijdschr Geneeskd 2004 30 oktober;148(44)
2189
15
16
17
18
Vries HG de, Niezen-Koning K, Kliphuis JW, Smit GP, Scheffer H,
Kate LP ten. Prevalence of carriers of the most common mediumchain acyl-CoA dehydrogenase (MCAD) deficiency mutation
(G985A) in the Netherlands. Hum Genet 1996;98:1-2.
Verkerk PH, Vaandrager GJ, Sengers RCA. Vijftien jaar landelijke
screening op fenylketonurie in Nederland; vierde verslag van de
Landelijke Begeleidingscommissie Phenylketonurie. Ned Tijdschr
Geneeskd 1990;134:2533-6.
Fromenty B, Mansouri A, Bonnefont JP, Courtois F, Munnich A,
Rabier D, et al. Most cases of medium-chain acyl-CoA dehydrogenase deficiency escape detection in France. Hum Genet 1996;
97:367-8.
Seddon HR, Green A, Gray RG, Leonard JV, Pollitt RJ. Regional
variations in medium-chain acyl-CoA dehydrogenase deficiency.
Lancet 1995;345:135-6.
19
20
21
22
Ruitenbeek W, Poels PJ, Turnbull DM, Garavaglia B, Chalmers
RA, Taylor RW, et al. Rhabdomyolysis and acute encephalopathy
in late onset medium chain acyl-CoA dehydrogenase deficiency.
J Neurol Neurosurg Psychiatry 1995;58:209-14.
Feillet F, Steinmann G, Vianey-Saban C, de Chillou C, Sadoul N,
Lefebvre E, et al. Adult presentation of MCAD deficiency revealed
by coma and severe arrythmias. Intensive Care Med 2003;29:1594-7.
Wilcken B, Carpenter KH, Hammond J. Neonatal symptoms in
medium chain acyl coenzyme A dehydrogenase deficiency. Arch Dis
Child 1993;69(3 Spec No):292-4.
Duran M, Hofkamp M, Rhead WJ, et al. Sudden child death and
‘healthy’ affected family members with medium-chain acyl-coenzyme
A dehydrogenase deficiency. Pediatrics 1986;78:1052-7.
Aanvaard op 30 juni 2004
Casuïstische mededelingen
Een fatale infectie door aviair influenza-A(H7N7)-virus en aanpassing van het
preventiebeleid*
s.a.g.kemink, r.a.m.fouchier, f.w.rozendaal, j.m.broekman, m.koopmans,
a.d.m.e.osterhaus en p.m.schneeberger
Trekkende watervogels vormen het natuurlijke reservoir van influenza-A-virussen.1 De virale eiwitten hemagglutinine en neuraminidase zijn belangrijke antigene
determinanten van het influenzavirus: bij wilde vogels
en pluimvee worden 15 subtypen van het hemagglutinine en 9 subtypen van het neuraminidase gevonden.2 De
subtypen H5 en H7 hebben de potentie om virulentiefactoren te verwerven bij de overstap van in het wild levende vogels naar pluimvee. Deze genetische veranderingen kunnen leiden tot voor vogels hoogpathogene
aviaire influenzavirussen, die vogelpestepidemieën kunnen veroorzaken.3
Mensen raken sporadisch geïnfecteerd door een aviair
influenzavirus. Vanwege hun eigenschap zich te kunnen
aanpassen aan replicatie bij de menselijke gastheer, zouden aviaire influenza-A-virussen aan de basis kunnen
staan van een humane pandemie.4 In 1997 werd in
Hongkong bij 18 personen een infectie vastgesteld door
*Een gedeelte van dit onderzoek werd eerder gepubliceerd in The
Proceedings of the National Academic Sciences of the United States of
America (2004;101:1356-61) met als titel ‘Avian influenza A virus
(H7N7) associated with human conjunctivitis and a fatal case of acute
respiratory distress syndrome.’
Jeroen Bosch Ziekenhuis, Nieuwstraat 34, 5311 NL ’s-Hertogenbosch.
Afd. Interne Geneeskunde: mw.dr.S.A.G.Kemink, internist.
Afd. Intensive Care: hr.F.W.Rozendaal, intensivist.
Afd. Pathologie: hr.J.M.Broekman, patholoog.
Laboratorium Medische Microbiologie: hr.dr.P.M.Schneeberger, artsmicrobioloog.
Erasmus Medisch Centrum, afd. Virologie, Nationaal Influenza Centrum, Rotterdam.
Hr.dr.R.A.M.Fouchier en hr.prof.dr.A.D.M.E.Osterhaus, virologen.
Rijksinstituut voor Volksgezondheid en Milieu, Diagnostisch Laboratorium voor Infectie Ziekten en Perinatale Screening, Bilthoven.
Mw.dr.M.Koopmans, viroloog.
Correspondentieadres: hr.dr.P.M.Schneeberger
2190
Ned Tijdschr Geneeskd 2004 30 oktober;148(44)
samenvatting
In februari 2003 was het voor vogels hoogpathogene aviaire
influenza-A(H7N7)-virus de oorzaak van een omvangrijke
uitbraak van vogelpest. Bij een 57-jarige mannelijke dierenarts
ontstond 2 dagen na een bezoek aan een pluimveebedrijf waar
vogelpest heerste, malaise, hoofdpijn en koorts. Na 8 dagen
werd hij in het ziekenhuis opgenomen met verschijnselen van
pneumonie. Vijf dagen later verslechterde zijn toestand in ernstige mate. Ondanks uitgebreide medicamenteuze behandeling
overleed hij 4 dagen nadien aan een acute pneumonie. In
eerder afgenomen bronchoalveolaire lavagevloeistof werd
met ‘reverse’-transcriptase(RT)-PCR influenza-A(H7N7)-virus
vastgesteld; de routineviruskweek leverde het isolaat A/Nederland/219/03 op, dat door 14 aminozuursubstituties verschilde
van het eerste isolaat bij de kip (A/kip/Nederland/1/03). Mede
op grond van deze casus werd het preventiebeleid aangepast;
personen die in contact kwamen met besmet gevogelte kregen
ruimere mogelijkheden voor vaccinatie en toepassing van oseltamivir.
aviair influenzavirus, subtype H5N1, van wie er 6 overleden.5 6 In februari 2003 raakten in China wederom
tenminste 2 mensen besmet door een vergelijkbaar
virus, van wie er 1 overleed.7
De overdracht van aviair influenza-A-virus van vogel
op mens is een potentieel bedreigende situatie voor de
volksgezondheid. In Nederland was er een uitbraak van
vogelpest door het aviair influenza-A(H7N7)-virus in
2003. Dat leverde een onverwacht hoog aantal transmissies van vogel naar mens op8 en leidde tot 1 sterfgeval.
De betreffende ziektegeschiedenis beschrijven wij in dit
artikel.
ziektegeschiedenis
Patiënt A, een 57-jarige mannelijke dierenarts, bezocht op 2
april 2003 beroepsmatig 5 pluimveebedrijven. Bij 1 van deze