Handleiding
Schrijven van teksten voor een richtlijn
Deze handleiding dient als leidraad en hulpmiddel tijdens het opstellen en schrijven van
evidence based richtlijnen. Deze manier van schrijven van teksten is een voorwaarde voor het
correct kunnen invoeren van de richtlijn in Oncoline. Het gebruik van deze handleiding leidt tot
een uniforme presentatie van de evidence based richtlijnen op Oncoline, dat betekent niet alleen
een uniforme lay-out, maar is ook de voorwaarde van een kwalitatief goede richtlijn.
Indeling van deze handleiding:
In het hoofdstuk Algemeen worden voorwaarde ten aanzien van de weergave beschreven.
In het Stappenplan bij het schrijven van de teksten wordt per stap de voorwaarde beschreven om
een inhoudelijk juiste weergave van het antwoord op de uitgangsvraag te geven.
Stap 1: Beschrijf per uitgangsvraag de literatuurbespreking (op basis van de evidence tabel)
Stap 2: Formuleer de conclusies met niveau van bewijs (o.b.v. literatuurbespreking en evidence
tabel)
Stap 3: beschrijf per uitgangsvraag de overige overwegingen
Stap 4: Formuleer per uitgangsvraag de aanbeveling op basis van de conclusie en overige
overweging
Algemeen
Lay-out van de teksten
De teksten dienen in het Nederlands in Word, lettertype Arial 10 volgens het Oncoline format te
worden geschreven.
Referenties
Literatuurverwijzing gebeurt in de tekst met de naam van de auteur tussen vierkante haken [ ..]. Maak
een literatuurlijst in alfabetische volgorde. De referenties worden hierin volgens de Vancouver-methode
genoteerd. Vermeld de gegevens compleet: auteur met initialen, titel artikel, tijdschrift, jaar, volume,
pagina.
Uitgangsvraag
De uitgangsvraag, namen auteurs en datum versie tekst dienen bovenaan de eerste pagina genoteerd
te worden.
Het bespreken van de teksten wordt vergemakkelijkt door het document te voorzien van pagina-en
regelnummering.
Regelnummering
- Klik in het menu Bestand op Pagina-instelling en klik vervolgens op het tabblad Indeling.
- Klik in het vak Toepassen op op Heel document
- Klik op Regelnummers.
- Schakel het selectievakje Regelnummers toevoegen in en selecteer vervolgens de gewenste opties.
Paginanummering
- Klik in het menu Invoegen op Paginanummers en klik vervolgens op OK.
Handleiding schrijven van teksten │© VIKC │MT │ juni 2010
1
Stappenplan bij het schrijven van de teksten
Het Oncoline format is als volgt opgebouwd:
literatuurbeschrijving (stap 1)
conclusies met niveau van bewijs (stap 2)
overige overwegingen (stap 3)
aanbevelingen (stap 4)
Stap 1: Literatuurbeschrijving
Onder het kopje ‘literatuurbeschrijving’ wordt de geselecteerde en beoordeelde literatuur kort
samengevat. De resultaten van de artikelen worden beschreven met daarbij ook indien van toepassing
(zie voorbeeld 1):
de grootte en/of de relevantie van de bevinding,
de grootte van de patiëntengroep
aantal studies
follow-up periode
de generaliseerbaarheid van de bevindingen
Grootte en/of relevantie van de bevinding:
Bij studies over een therapie:
Het relatief risico of odds ratio (met 95% betrouwbaarheidsintervallen) dient gebruikt te worden. Het
samenvatten van de resultaten in termen van ‘significant beter’ of ‘niet significant verschillend’ moet
vermeden worden, alsmede het geven van P-waardes.
Bij studies over diagnostiek:
Indien het gaat om het vergelijken van het onderscheidend vermogen van meerdere testen kan
rapportage gebeuren met sensitiviteit en specificiteit of met likelihood ratios. De mate van
onzekerheid van deze parameters moet ook weergegeven worden met 95%
betrouwbaarheidsintervallen. Ook moet aangegeven worden wat de verwachte gezondheidswinst of
kostenbesparing is.
Soms worden diagnostische testen geëvalueerd in studies waarin een bepaalde testuitslag gevolgd
wordt door een interventie. In deze gevallen is het mogelijk de waarde van de diagnostische test te
bepalen aan de hand van verschillen in gezondheidsuitkomst (relatief risico of odds ratio met 95%
betrouwbaarheidsintervallen).
Per uitgangsvraag wordt door de methodologische expert die het literatuuronderzoek heeft gedaan een
samenvatting van de literatuur weergegeven in de CoCanCPG evidence tabel ‘treatment’, ‘diagnosis’ of
‘prognosis’. Deze evidence tabellen zijn in het Engels ingevuld en wordt door de procesbegeleider aan
de betreffende subwerkgroep gegeven.
Voorbeeld 1: Omschrijving literatuur
In de EORTC studie 22863 werden 415 patiënten ingesloten met een cT1-2 graad III tumor (9%) of
patiënten met een cT3-4 graad I-III tumor [Bolla 1997, 2002]. Alle patiënten ontvingen 70 Gy
conventionele radiotherapie. In de combinatie arm werden gosereline 4-wekelijkse injecties gestart
op de eerste dag van de radiotherapie en drie jaar gecontinueerd. Cyproteronacetaat (150 mg oraal)
werd gegeven voor 1 maand en werd gestart 1 week voor de eerste gosereline injectie. Na een
mediane follow-up van 66 maanden was er in deze studie een significant verschil in de 5-jaars
ziektevrije (74 versus 40%) en algehele overleving (78 versus 62%) in het voordeel van de
combinatiebehandeling.
Handleiding schrijven van teksten │© VIKC │MT │ juni 2010
2
Stap 2: Conclusies met niveau van bewijs
Let op: er circuleren diverse versies van tabellen met definities van level of evidence. Dit is de enige
juiste!
Formuleer op basis van de literatuur één of meerdere conclusies welke het meest relevant zijn voor het
beantwoorden van de vraag. Geef per conclusie de belangrijkste literatuur weer. Gradeer de literatuur
naar mate van bewijs (zie tabel 3, 4 5 en voorbeeld 2). In tabel 3 wordt tevens weergegeven hoe de
conclusie op basis van level of evidence geformuleerd kunnen worden. Alle literatuur die in de conclusie
is opgenomen dient te zijn beschreven in de literatuuromschrijving.
Tabel 3: Niveau van bewijskracht van de conclusie op basis van het aan de conclusie ten
grondslag liggend bewijs
Niveau
van bewijs
1
2
3
4
Conclusie gebaseerd op
Formulering
1 systematische review (A1) of tenminste 2
onafhankelijk van elkaar uitgevoerde onderzoeken
van niveau A1 of A2
tenminste 2 onafhankelijk van elkaar uitgevoerde
onderzoeken van niveau B
1 onderzoek van niveau A2, B of C
Het is aangetoond dat…; men
dient…
Mening van deskundigen (bijvoorbeeld de
werkgroepleden)
Het is aannemelijk dat…; men
zou…moeten…
Er zijn aanwijzingen dat…; men
kan…
De werkgroep is van mening
dat…
Tabel 4: Diagnostische tests
Indeling van onderzoeksresultaten naar mate van bewijskracht
A1
onderzoek naar de effecten van diagnostiek op klinische uitkomsten bij een prospectief
gevolgde goed gedefinieerde patiëntengroep met een tevoren gedefinieerd beleid op
grond van de te onderzoeken testuitslagen, of besliskundig onderzoek naar de effecten
van diagnostiek op klinische uitkomsten, waarbij resultaten van onderzoek van A2-niveau
als basis worden gebruikt en voldoende rekening wordt gehouden met onderlinge
afhankelijkheid van diagnostische test;
A2
Onderzoek ten opzichte van een referentietest, waarbij van tevoren criteria zijn
gedefinieerd voor de te onderzoeken test en voor een referentietest, met een goede
beschrijving van de test en de onderzochte klinische populatie; het moet een voldoende
grote serie van opeenvolgende patiënten betreffen, er moet gebruik gemaakt zijn van
tevoren gedefinieerde afkapwaarden en de resultaten van de test, en de ‘gouden
standaard’ moeten onafhankelijk zijn beoordeeld. Bij situaties waarbij multiple,
diagnostische test een rol spelen, is er in principe een onderlinge afhankelijkheid en dient
de analyse hierop te zijn aangepast, bijvoorbeeld met logistische regressie;
B
Vergelijking met een referentietest, beschrijving van de onderzochte test en van de
onderzochte populatie, maar niet de kenmerken die verder onder niveau A staan
genoemd.
C
Niet-vergelijkend onderzoek
D
Mening van deskundigen (bijvoorbeeld werkgroepleden)
Handleiding schrijven van teksten │© VIKC │MT │ juni 2010
3
Tabel 5: Interventiestudies (preventie of therapie)
Indeling van onderzoeksresultaten naar mate van bewijskracht
A1
Systematische reviews die tenminste enkele onderzoeken van A2-niveau betreffen, waarbij de
resultaten van afzonderlijke onderzoeken consistent zijn.
A2
Gerandomiseerd vergelijkend klinisch onderzoek van goede kwaliteit en met voldoende
omvang en consistentie.
B
Gerandomiseerde klinische trials van matige kwaliteit of onvoldoende omvang of ander
vergelijkend onderzoek (niet-gerandomiseerd: vergelijkend cohortonderzoek, patiënt-controleonderzoek)
C
Niet-vergelijkend onderzoek
D
Mening van deskundigen (bijvoorbeeld de werkgroepleden)
Voorbeeld 2: Conclusie met niveau van bewijs
TE VERWACHTEN UITKOMSTEN BIJ (NEO)ADJUVANTE HORMONALE THERAPIE
Er zijn onvoldoende aanwijzingen dat (neo)adjuvante hormonale therapie bij patiënten met
gelokaliseerd prostaatcarcinoom bijdraagt aan de overlevingskans van de patiënt. Dit geldt in nog
sterkere mate voor de laag en matige risicogroep.
Niveau 2: B Roach 2003 [188], Ciezki 2004 [185] Merrick 2005 [187]
Als er een indicatie voor aanvullende hormonale therapie wordt gesteld, dan lijkt een kortdurende
behandeling van zes maanden voldoende.
Niveau 4
Handleiding schrijven van teksten │© VIKC │MT │ juni 2010
4
Stap 3: Overige overwegingen
Op basis van de conclusie(s) worden aanbevelingen geformuleerd. Echter, naast de evidence uit de
literatuur zijn er andere overwegingen (zie voorbeeld 3) die meespelen bij het formuleren van de
aanbeveling.
De ‘Overige overwegingen’ worden onder een apart kopje in het oncoline format vermeld. Op deze
manier wordt duidelijk hoe de werkgroep tot een bepaalde aanbeveling is gekomen. Denk bij het
formuleren van de overige overwegingen aan de volgende onderwerpen beschreven in onderstaande
tabel ‘checklist overige overwegingen’:
Tabel Checklist overige overwegingen
Items
A)
Formuleer of het
van belang is en
hoe
1. Veiligheid
Ja/Nee
Indien ja: hoe
B)
Prioritering
t.a.v. belang
van 1-6
C)
Meenemen in
opstellen
aanbeveling?
□ Ja
□ Nee
D)
Indien meenemen in aanbeveling:
Versterkt of verzwakt
de overweging de conclusie?
□ Versterkt
□ Neutraal
□ Verzwakt, blijft zelfde richting
□ Verzwakt, verandert v richting
2. Patiënten
perspectief
Ja/Nee
Indien ja: hoe
□ Ja
□ Nee
□ Versterkt
□ Neutraal
□ Verzwakt, zelfde richting
□ Verzwakt, verandert v richting
3. Professioneel
perspectief
Ja/Nee
Indien ja: hoe
□ Ja
□ Nee
□ Versterkt
□ Neutraal
□ Verzwakt, blijft zelfde richting
□ Verzwakt, verandert v richting
4. Kosten
effectiviteit
Ja/Nee
Indien ja: hoe
□ Ja
□ Nee
□ Versterkt
□ Neutraal
□ Verzwakt, blijft zelfde richting
□ Verzwakt, verandert v richting
5. Organisatie
Ja/Nee
Indien ja: hoe
□ Ja
□ Nee
□ Versterkt
□ Neutraal
□ Verzwakt, blijft zelfde richting
□ Verzwakt, verandert v richting
6. Maatschappij
Ja/Nee
Indien ja: hoe
□ Ja
□ Nee
□ Versterkt
□ Neutraal
□ Verzwakt, blijft zelfde richting
□ Verzwakt, verandert v richting
Uitleg items checklist (De items kunnen beoordeeld worden m.b.v.
richtlijnwerkgroep, b literatuuronderzoek, c patiëntenenquêtes/interviews
a
professionals in de
1.
-
Veiligheidsissues. Dit betreft o.a. aspecten die in de evidence tabel niet aan de orde komen, zoals
Bijwerkingen, risico’s of complicaties op korte en lange termijn (a, b)
Gebruik bij co-morbiditeit / gelijktijdig gebruik medicatie en/of interventie (a,b)
2.
-
Patiëntenperspectief. Aspecten die in het kader hiervan bekeken kunnen worden:
Behoefte en verwachtingen / voorkeuren / te verwachten compliance / te verwachten tevredenheid /
kwaliteit van leven (a, b, c)
3.
-
Professioneel perspectief. Aspecten die in het kader hiervan bekeken kunnen worden:
Risico’s die professional loopt bij het toepassen van de interventie / tijdbesparing of het verlies aan
tijd door het invoeren van de interventie (a, b)
Klinische autonomie / bereidheid toepassen (nieuwe kennis en vaardigheden) / houding, normen en
waarden van de professional (a)
-
4.
-
Kosten effectiviteit:
Kosteneffectiviteit in verhouding tot bestaande ingrepen/behandelingen voor deze ziekte (a, b)
5.
Organisatorische factoren.
Handleiding schrijven van teksten │© VIKC │MT │ juni 2010
5
-
De beschikbaarheid faciliteiten & medicijnen / de wijze waarop de organisatie van de zorg
aangeboden dient te worden / grootte van de verandering in de organisatie-zorgproces /
infrastructuur voor implementatie (a)
6.
Factoren die een rol spelen op het niveau van de maatschappij. Aspecten die in het kader hiervan
bekeken kunnen worden:
Hoe groot is het probleem (in aantallen), hoe verhouden de kosten zich t.o.v. kosten van andere
ingrepen/behandelingen in het kader van andere ziekten (a, b)
Vergoeding door verzekeraars / ethische overwegingen / juridische overwegingen / politieke en
strategische consequenties / industriële belangen (a)
-
Voorbeeld 3 : Overige overwegingen
TE VERWACHTEN UITKOMSTEN BIJ RADICALE PROSTECTOMIE
Resultaten zijn afhankelijk van T-stadium, iPSA en Gleasonscore en van de chirurgische ervaring.
Bedacht moet worden dat alle grote series resultaten geven van patiënten die behandeld werden in de
tijd dat er nog geen uitgebreide stagering mogelijk was door beperkte beeldvorming, nog niet bekend
zijn van PSA-bepalingen en ontbreken van de Gleason indeling.
De resultaten van zenuwsparende, laparoscopische en robottechnieken zullen in de loop der jaren
moeten bewijzen gelijkwaardig te zijn aan die van de klassieke prostatectomie.
De rol en uitgebreidheid van de lymfeklierdissectie bij het prostaatcarcinoom zijn op dit moment
onderwerp van discussie.
Handleiding schrijven van teksten │© VIKC │MT │ juni 2010
6
Stap 4: Aanbevelingen
Veelal worden in de richtlijn alleen de aanbevelingen gelezen. De aanbevelingen dienen daarom als
volgt gedefinieerd te worden:
Aanbevelingen kunnen op zichzelf staand worden gelezen
Aanbevelingen beantwoorden de uitgangsvraag
Aanbevelingen zijn specifiek en ondubbelzinnig.
Er bestaat een expliciet verband tussen de aanbevelingen en het onderliggende
wetenschappelijke bewijs
De sterkte van de formulering van een aanbeveling dient te worden vastgesteld aan de hand
van de ‘level of evidence’ en overige overwegingen (zie tabel 6, voorbeeld 4).
In medisch, maatschappelijk of juridisch opzicht kunnen aanbevelingen een normatief karakter hebben.
Dit hangt ondermeer af van de formulering van de aanbevelingen. De formulering van een aanbeveling
dient dan ook zorgvuldig te worden gekozen en te worden gebaseerd op de sterkte van de bewijskracht
van het wetenschappelijke bewijs en overige overwegingen. Andere overwegingen kunnen o.a. zijn:
klinische relevantie, schade of bijwerkingen, de beschikbaarheid van middelen, de kosten en organisatie
van de zorg, patiëntenperspectief en ethische aspecten.
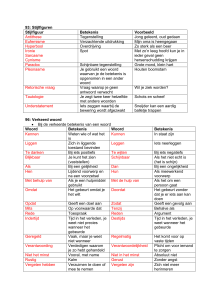
Tabel 6: Voorkeursformuleringen voor een aanbeveling
Sterkte van de aanbeveling
sterk
Matig sterk
Zwak
Geen
voorkeursformulering
Positieve aanbeveling
Negatieve aanbeveling
- sterk aan te bevelen
- sterk te ontraden
- dient/moet
- dient niet/moet/niet
- is eerste keuze
- is geen keuze
- is geïndiceerd
- is gecontraindiceerd
- is vereist
- is de standaard
- aan te bevelen
- niet aan te bevelen
- adviseren
- wordt ontraden
- heeft de voorkeur
- verdient geen aanbeveling
- streven naar
- verdient aanbeveling
- te overwegen
- is wellicht geen plaats
- is een optie
- lijkt niet zinvol
- kan
- is terughoudendheid
- er is mogelijk plaats
geboden
- kan zinvol zijn
- kan geen advies of aanbeving worden gegeven
- niet mogelijk een keuze te maken
- er is geen voorkeur uit te spreken
Voorbeeld 4: Aanbevelingen
LYMFEKLIERDISSECTIE
Er dient een lymfeklierdissectie te worden geïndiceerd als het resultaat
consequenties heeft voor de uiteindelijke behandeling. Een risicoschatting op
de aanwezigheid van positieve lymfeklieren wordt gemaakt op basis van
onder andere de Kattan nomogrammen.
Handleiding schrijven van teksten │© VIKC │MT │ juni 2010
7