6.1 – DEELTJES, WATER, IJS EN LUCHT - BEGRIJPEN
Wolken
- Bestaan uit zwevende
waterdruppeltjes (mist)
- Hoe groter de druppels, hoe
donkerder de kleur
Ontstaan van wolken
Water verdamping waterdamp
(onzichtbaar gas) stijgt om hoog
lucht wordt koud minder
waterdamp dan in warme lucht
waterdruppeltjes wolken
Sneeuw
Als het hoog in de lucht vriest bevriest
de waterdamp en ontstaan er
ijskristallen die groeien aan tot
sneeuwvlokken
Hagelsteen
Sneeuwvlok omringd door bevroren
waterdruppels
Ontstaan hagelstenen
- Een hoge donkere wolk
bovenin: onder het vriespunt
sneeuwvlokken vallen door
de wolk naar beneden
druppels water vriezen als ijs
aan de sneeuwvlok vast
hagelsteen
- Grotere hagelstenen ontstaan
als tijdens het vallen meerdere
hagelstenen aan elkaar vast
vriezen
IJzel
Regen die valt op een bevroren grond
en vast vriest
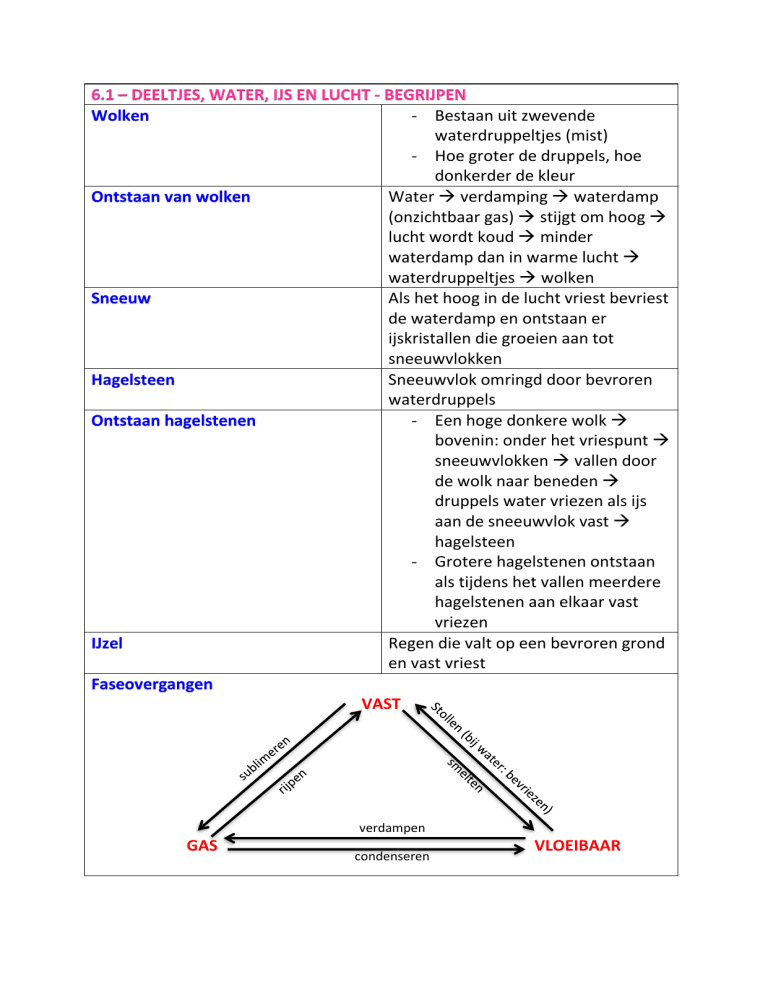
Faseovergangen
VAST
verdampen
GAS
condenseren
VLOEIBAAR
- Een vloeistof verandert razend
snel in een gas
- Er ontstaan overal in de
vloeistof gasbellen
6.1 – DEELTJES, WATER, IJS EN LUCHT – VERKLAREN
Moleculen
- Kleine deeltjes waaruit stoffen
bestaan
- Te klein om te kunnen zien (ook
niet met een microscoop)
Atomen
Bouwstenen van een molecuul
Eigenschappen moleculen
- Ze verschillen in grootte (altijd
onzichtbaar)
- Ze verschillen in massa
- Ze trekken elkaar aan
- Ze bewegen altijd (hoe warmer,
hoe sneller)
Eigenschap per fase
Gas
- Geen aantrekkingskracht
- Snelle beweging
Vloeibaar
- Wel aantrekkingskracht
- Bewegen door elkaar heen
Vast
- Veel aantrekkingskracht
- Trilling rondom een vast punt
Afkoringen elementen
6.2 – ZWAAR EN LICHT – BEGRIJPEN
Dichtheid
- de massa een blokje van één
cm3
- word gebruikt om te vergelijken
hoe zwaar stoffen zijn
- als de dichtheid van het
Drijven en zinken
voorwerp lager is dan de
dichtheid van de vloeistof dan
blijft het drijven
- dichtheid hoger? zinken
Zweven
dichtheid voorwerp en dichtheid
vloeistof is gelijk
Kookpunt
Dichtheid gas
Zout water
Zeestroming
6.2 – ZWAAR EN LICHT – BEREKENEN
Formule massa
Formule dichtheid
- afhankelijk van de temperatuur
- word uitgedrukt in g/m3 omdat
gassen erg licht zijn
heeft een hogere dichtheid dan zoet
water
- worden gevolgd met behulp
van de dichtheid van water
- dichtheid van wat is afhankelijk
van temperatuur en
zoutgehalte
- 𝑀𝑎𝑠𝑠𝑎 (𝑔) = 𝑑𝑖𝑐ℎ𝑡ℎ𝑒𝑖𝑑 (𝑔/
𝑐𝑚3) × 𝑣𝑜𝑙𝑢𝑚𝑒 (𝑐𝑚3)
- 𝑚 = 𝜌 × 𝑉
𝑚𝑎𝑠𝑠𝑎
- 𝑑𝑖𝑐ℎ𝑡ℎ𝑒𝑖𝑑 =
- 𝜌=
Formule volume
Volume onregelmatig voorwerp
6.3 – IN DE LUCHT – BEGRIJPEN
Samenpersen
Warme lucht
𝑉
- 𝑣𝑜𝑙𝑢𝑚𝑒 =
- 𝑉=
Volume vloeistoffen
𝑚
𝑚
𝑣𝑜𝑙𝑢𝑚𝑒
𝑚𝑎𝑠𝑠𝑎
𝑑𝑖𝑐ℎ𝑡ℎ𝑒𝑖𝑑
𝜌
- 𝑉 = 𝑙𝑒𝑛𝑔𝑡𝑒 × 𝑏𝑟𝑒𝑒𝑑𝑡𝑒 ×
ℎ𝑜𝑜𝑔𝑡𝑒
- Gegeven in liters
- 1 L = 1 dm3
- Figuur 43 blz. 237
- Meer massa in het zelfde
volume stoppen
- Dichtheid van een gas staat niet
vast
- Je kunt een gas samenpersen
- Vloeistoffen en vaste stoffen
kun je niet samen persen
zonder dat het van vorm
veranderd
- Kleinere dichtheid dan koude
lucht (door snel bewegende
deeltjes)
- Stijgt op
Druk
Constante druk
Temperatuur en druk
Vacuüm
IJler
6.3 – IN DE LUCHT – BEREKENEN
Eenheid luchtdruk
Formule luchtdruk en kracht
F (kracht)
p (druk)
A (oppervlakte)
Eenheid voor luchtdruk
Barometer
Manometer
Onderdruk
- Door het bewegen en botsen
van luchtdeeltjes ontstaat druk
- Hoe meer deeltjes hoe hoger de
druk
Heel veel deeltjes die heel vaak
botsen
Hoge temperatuur sneller bewegen
meer botsingen hogere druk
Een ruimte waar helemaal niets is
- Minder luchtdeeltjes in een m3
- Hoog in de bergen
- Moelijker ademhalen
- N/m2
- 1 N/cm2 = 10.000 N/m2
𝑘𝑟𝑎𝑐ℎ𝑡 = 𝑑𝑟𝑢𝑘 × 𝑜𝑝𝑝𝑒𝑟𝑣𝑙𝑎𝑘𝑡𝑒
𝐹 =𝑝×𝐴
- N
- N/cm2
- cm2
- bar
1 bar = 10 N/cm2
1 bar = 100.000 N/cm2
1 bar = 1000 mbar (millibar)
meet de luchtdruk in millibars
Meet het verschil tussen de gasdruk
binnen en luchtdruk buiten
Als de druk in een ruimte lager is dan
normaal (er is lucht weg gepompt)












