Concordantietabel voor het eerste jaar van de 2de graad TSO
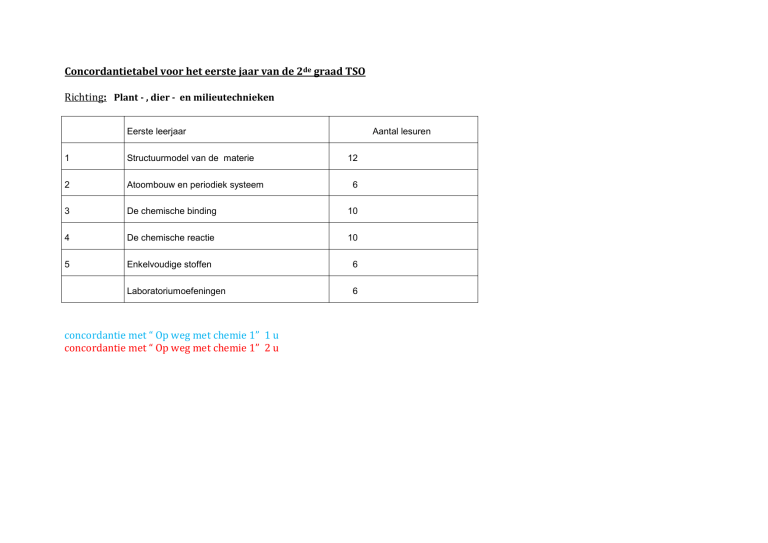
Richting: Plant - , dier - en milieutechnieken
Eerste leerjaar
Aantal lesuren
1
Structuurmodel van de materie
2
Atoombouw en periodiek systeem
3
De chemische binding
10
4
De chemische reactie
10
5
Enkelvoudige stoffen
6
Laboratoriumoefeningen
6
concordantie met “ Op weg met chemie 1” 1 u
concordantie met “ Op weg met chemie 1” 2 u
12
6
Het structuurmodel van de materie ( 12 u)
LEERPLANDOELSTELLINGEN
LEERINHOUDEN
1
Een onderscheid maken
stofeigenschappen.
tussen
voorwerp-
en
Materie
2
De begrippen 'homogene mengsels' en 'heterogene
mengsels' omschrijven en in duidelijke gevallen
herkennen.
Soorten mengsels
3
Verwoorden dat zuivere stoffen welbepaalde fysische
karakteristieken bezitten.
Zuivere stoffen
4
Verduidelijken dat zuivere stoffen bekomen worden
door toepassing van scheidingstechnieken op
mengsels.
Scheidingstechnieken
5
Samengestelde en enkelvoudige stoffen van elkaar
onderscheiden op grond van het al dan niet
afbreekbaar zijn tot andere stoffen (met andere
stofeigenschappen).
Enkelvoudige en
samengestelde
stoffen
6
Een deeltjesmodel hanteren om zich de bouw van de
materie voor te stellen.
Deeltjesmodel
7
Aan de hand van een deeltjesmodel enkelvoudige en
samengestelde stoffen van elkaar onderscheiden
Op weg met
chemie 1u
8-15
Op weg met
chemie 2u
10 - 14
22 - 25
24 - 27
14
26 - 27
16
28 - 29
27 – 33
30 - 37
46 – 48
58 - 60
49
61
62 - 63
77 – 79
Atoombouw en periodiek systeem
LEERPLANDOELSTELLINGEN
LEERINHOUDEN
8
Een atoom beschrijven als samengesteld uit protonen,
neutronen en elektronen en hun 'plaats' binnen het
atoom omschrijven.
Samenstelling van het
atoom
Inleiding
tot
het
atoommodel van Bohr
9
Een element omschrijven als een atoomsoort bepaald
door het aantal protonen per atoom zoals weergegeven door het atoomnummer en voorgesteld door
een eigen chemisch symbool.
Element en chemisch
symbool
10
Het periodiek systeem der elementen beschrijven als
een ordening volgens bepaalde criteria.
Periodiek systeem der
elementen (PSE)
11
De periodiciteit weergeven voor de elementen van de
hoofdgroepen.
- periodiciteit
12
De begrippen periode en groep in het PSE hanteren.
- hanteren van het
PSE
Op weg met
chemie 1u
55 – 59
96 - 103
Op weg met
chemie 2u
68 – 70
120 - 128
59
74
114
138
114 - 116
138 - 140
115
139
Op weg met
chemie 1u
116
Op weg met
chemie 2u
140 141
133 - 141
159 - 167
De chemische binding
LEERPLANDOELSTELLINGEN
LEERINHOUDEN
13
De elektronenconfiguratie van de edelgasatomen in
verband brengen met hun stabiliteit.
Stabiliteit van
edelgasatomen
14
Aan de hand van eenvoudige voorbeelden het
ontstaan van drie bindingstypes illustreren als een
streven naar de edelgasconfiguratie.
Bindingstypes:
- ionbinding
- covalente binding
- metaalbinding
15
Een rooster omschrijven als een logische verzameling
van ionen, atomen of moleculen.
Roosters
16
Het verband tussen bindingstype en fysische
eigenschappen bij binaire verbindingen verwoorden.
Bindingstype en
fysische eigenschappen
Het begrip oxidatiegetal omschrijven.
Oxidatiegetal
17
135 +138+139
161+164+165
167 - 169
136
162
165 – 167
139 - 140
De chemische reactie
Op weg met
chemie 1u
LEERPLANDOELSTELLINGEN
LEERINHOUDEN
Verwoorden dat chemische reacties processen zijn
waarbij andere stoffen gevormd worden en die
gepaard gaan met energieomzettingen.
Vorming van andere
stoffen
48
19
Een chemische reactie
herschikking van atomen.
Herschikking van
atomen
72 - 73
20
De wet van massabehoud
verduidelijken als een logisch
herschikking van atomen.
21
De symbolische schrijfwijze van een eenvoudige
chemische reactie interpreteren als een herschikking
van atomen.
Reactievergelijking
interpreteren
22
Eenvoudige reactievergelijkingen voor reacties tussen
enkelvoudige stoffen opstellen.
opstellen
23
Het onderscheid tussen exo- en endo-energetische
reacties aangeven.
Energie-effecten
18
voorstellen
als
een
verwoorden en
gevolg van een
Wet van
massabehoud
Op weg met
chemie 2u
60
94 - 95
77 - 78
88 – 89
74 - 75
90 – 91
79 - 81
100 – 101
79 - 81
100 - 101
77 - 78
94 - 95
Enkelvoudige stoffen
Op weg met
chemie 1u
62
Op weg met
chemie 2u
77
Eigenschappen
139 – 140
88 – 89
108 - 110
165 – 167
Toepassingen
87 – 89
127 – 129
146 - 148
108 – 111
LEERPLANDOELSTELLINGEN
LEERINHOUDEN
24
Van een enkelvoudige stof de symbolische schrijfwijze
interpreteren en een juiste benaming geven.
Symbolische
schrijfwijze
Benaming
25
Enkele eigenschappen met inbegrip van het normaal
voorkomen
(aggregatietoestand)
van
enkele
enkelvoudige stoffen verwoorden.
26
Enkele toepassingen
verwoorden.
27
van
enkelvoudige
stoffen
Tabellen met R- en S-zinnen gebruiken en de
betekenis van de gevaarsymbolen verwoorden.
R- en S-zinnen
Gevaarsymbolen
166
196 - 207
210 -211












