Natuurlijke radioactiviteit
Met natuurlijke radioactiviteit wordt bedoeld: radioactiviteit die niet kunstmatig is opgewekt.
Kernen die labiel zijn “vervallen” zodat ze veranderen in een kern van een ander element.
1. Bètastraling
Betastraling bestaat uit snel bewegende elektronen. Deze elektronen komen uit de
atoomkern. Hoe kan dat? Er zitten toch geen elektronen in de kern?
Een voorbeeld
Thorium (Th) met atoommassa 231 kan veranderen in Protactinium (Pa)
Dit proces wordt β-verval (beta decay) genoemd.
In de kern gebeurt het volgende: een neutron splitst zich in een proton en een elektron.
n p+e
Het proton blijft in de kern. Het elektron vliegt weg met hoge snelheid.
Dit wordt bètastraling genoemd.
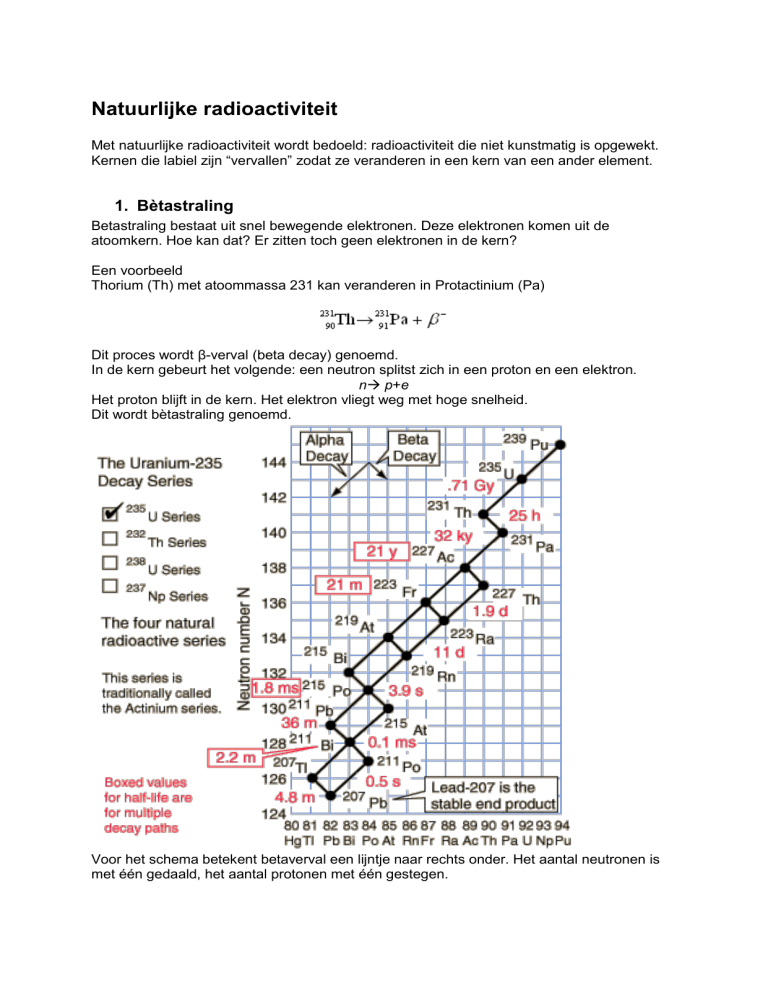
Voor het schema betekent betaverval een lijntje naar rechts onder. Het aantal neutronen is
met één gedaald, het aantal protonen met één gestegen.
2. Alfastraling.
Alfa straling bestaat uit snel bewegende heliumkernen. Een heliumkern
bestaat uit twee protonen en twee neutronen. Als dit groepje deeltjes een
atoomkern uitvliegt spreken we van α-straling.
In het vervalschema (z.o.z.) komt dit overeen met een lange streep naar
linksonder.
Het aantal protonen en het aantal neutronen daalt met twee.
Voorbeeld:
K-vangst.
Een volgende kernreactie heet K-vangst. In het engels wordt dit electron-capture genoemd.
Een atoomkern kan labiel zijn omdat het aantal protonen relatief hoog is.
Een elektron kan dan uit de K-schil in de kern vallen. Samen met een proton wordt dan een
extra neutron gevormd:
p+e n
Zoals je ziet daalt hierbij het aantal protonen en stijgt het aantal neutronen met één.
Ook verdwijnt er een elektron maar die zal het betreffende atoom wel weer ergens vandaan
halen.
Voorbeeld:
Applet
Onderstaande applet laat verschillende isotopen zien. De labiele isotopen vervallen tot
andere elementen.
http://www.colorado.edu/physics/2000/applets/iso.html
3. Gammastraling
Gammastraling (γ) is elektromagnetische straling. Het bestaat dus niet uit “deeltjes” zoals α en β-straling.
De golflengte is zeer klein, de frequentie en dus ook de energie per foton zijn zeer hoog.
Bij kernreacties zorgt de gammastraling ervoor dat wetten van massa- en energiebehoud
kloppen.
4. Halveringstijd
Met halveringstijd van radioactief materiaal wordt bedoeld:
De tijd die nodig is om het aantal kernen tot de helft te laten afnemen.
Bijvoorbeeld: De halveringstijd van
is 4,0 uur
Dat betekent dat na 4,0 uur nog maar de helft over is. Na nog 4,0 uur een kwart. (de helft
van de helft).
Met onderstaande formule is het aantal kernen Nt op tijdstip t te berekenen als het
beginaantal N0 is en de halveringstijd
5. Vragen over kernreacties:
1. Wat wordt er bedoeld met Electron Capture?
Geef een voorbeeld.
2. Wat wordt er bedoeld met Betha decay?
Geef een voorbeeld.
3. Kernreacties kloppend maken
14
C 14 N +……..
22
Mg +
22 Na
210
Po …..+ α
238
U 234 Th + ……
4. Wat heeft α-straling met Helium te maken?
5. Zoek de halveringstijd op van technetium
.
Van deze stof wordt 5,0 mg bij een patiënt ingespoten.
Bereken hoeveel er over is na 4,5 uur.
6. Zoek de halveringstijd op van koolstof- 14:
Hoeveel neutronen bevinden zich in de kern?
Bereken hoeveel % er over is na 10000 jaar.
7. Hiernaast zie je een grafiek
Lees af: het beginaantal en de de
halfwaardetijd
Geef de formule voor Nt die bij deze
grafiek hoort.
.












