Een kort overzicht van Galapagos
Galapagos is een drug discovery onderneming gericht op het vinden van nieuwe medicijnen
tegen ziekten die gewrichten en botten aantasten. Deze samenvatting geeft een beknopte
introductie tot Galapagos’ technologie en zet uiteen hoe zijn unieke aanpak kan helpen
nieuwe medicijnen naar de markt te brengen.
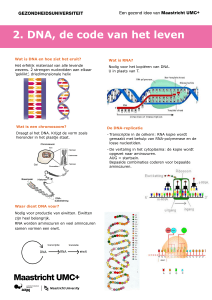
Het menselijke genoom, de blauwdruk voor alle cellen in het menselijk lichaam, bestaat uit
tienduizenden genen. Genen zijn opgebouwd uit DNA en bevatten de instructies voor de
productie van alle eiwitten in de cel. Eiwitten reguleren de structuur en functie van alle cellen
die samen het menselijke lichaam vormen. Voordat een cel het DNA kan gebruiken om eiwit te
maken, moet het DNA eerst herschreven worden in RNA. Het mechanisme van de cel gebruikt
vervolgens het RNA om eiwit te produceren. Het proces van de productie van eiwitten in de cel
gaat dus van DNA naar RNA naar eiwit (zie het gele kader in Figuur 1).
Vrijwel alle ziekten en afwijkingen worden veroorzaakt door een verstoring in de normale
werking van bepaalde eiwitten. Het belangrijkste doel van farmaceutische bedrijven is daarom
het ontwerpen van medicijnen die de activiteit van deze eiwitten zodanig veranderen, dat de
normale werking terugkeert en de oorzaak van de ziekte wordt geminimaliseerd of
uitgeschakeld. Eén van de belangrijkste obstakels in het ontdekken van nieuwe medicijnen is
exact te weten welke van de duizenden eiwitten in het lichaam een sleutelrol spelen in een
bepaalde ziekte. Wanneer deze eiwitten zijn ontdekt, worden zij targets voor het ontwerp van
een medicijn. Het vinden van deze targets is één van de kritische stappen in het proces van de
ontdekking van geneesmiddelen.
Om eiwitten in menselijke cellen te bestuderen, maakt Galapagos gebruik van de
kenmerkende eigenschappen van adenovirussen. Het adenovirus is het virus dat de gewone
verkoudheid veroorzaakt en is in staat om vrijwel elk type menselijke cel te infecteren,
hetgeen de reden is dat het zo besmettelijk is. De adenovirussen waar Galapagos mee werkt,
zijn ontworpen om als transportmiddel te dienen voor het inbrengen van specifieke stukken
DNA in menselijke cellen. Daarnaast zijn deze virussen ongeschikt gemaakt voor replicatie.
Dit betekent dat zij niet in staat zijn om zich buiten de laboratoriumomgeving te reproduceren
en daarom een veilig middel zijn voor het inbrengen van DNA in menselijke cellen. Figuur 1
toont hoe de virussen deze stukken DNA in menselijke cellen in de laboratoriumomgeving
inbrengen, waardoor de cellen ofwel meer produceren van een bepaald eiwit (knock-in),
ofwel de productie van nieuw eiwit blokkeren (knock-down).
KnockKnock-down
KnockKnock-in
SilenceSelect®
FLeXSelect®
Knock-down vs knock-in
DNA
DNA
DNA
RNA
RNA
RNA
eiwit
eiwit
eiwit
hoeveelheid eiwit
in normale cellen
hoeveelheid eiwit
na knock
knock--down
hoeveelheid eiwit
na knock
knock--in
Figuur 1: Vergelijking van de hoeveelheid van een bepaald
eiwit voor en na knock-in of knock-down.
Knock-down virussen werken door kleine
stukken RNA (siRNA) te maken, die zich
bindt aan een specifieke RNA sequentie
die een bepaald eiwit produceert. Nadat
het siRNA het RNA bindt, wordt het RNA
door het mechanisme van de cel
opgesplitst, waardoor de productie van
het eiwit door het RNA wordt gestopt. Dit
proces wordt RNA-interferentie (RNAi)
genoemd en leidt tot een vermindering
van de hoeveelheid van het betreffende
eiwit.
Bij de knock-in virussen wordt een
specifiek stuk DNA (dat de instructies
bevat om een bepaald eiwit te maken) in
het virus ingebracht. Nadat het virus de
cel geïnfecteerd heeft, begin de cel meer
te produceren van het corresponderende
eiwit.
Galapagos combineert de mogelijkheid om de hoeveelheid eiwit in menselijke cellen te
veranderen met een high-throughput screening methode. Door gebruik te maken van deze
methode is Galapagos in staat om vele kleine schaal experimenten gelijktijdig uit te voeren.
Galapagos maakt gebruik van een rastersysteem, waarbij iedere punt op het raster
overeenkomt met een klein testbuisje met cellen die een wijziging in een specifiek eiwit
hebben ondergaan. Hierdoor kan Galapagos in een korte periode vele duizenden eiwitten
screenen.
Virussen die specifiek e stuk jes DNA bevatten
worden gerangschik t op een raster.
Ieder virus introduceert dit specifiek e stuk je
DNA in cellen
cellen,, waardoor een k nock -in of
k nock -down van een bepaald eiwit wordt
veroorzaak t.
t. Hierdoor bevat ieder vierk ant op
het raster cellen die een veranderde
hoeveelheid van éé
één
n bepaald eiwit hebben.
hebben.
Experimenten worden ont worpen om te
bepalen (door middel van bijvoorbeeld een
k leurverandering)
leurverandering) wat het effect is van de
eiwitverandering op de cellen
cellen.. Omdat deze
verandering samenhangt met een specifiek
eiwit,, k an dit eiwit verder worden onderzocht
eiwit
en uiteindelijk een target voor een medicijn
worden..
worden
Figuur 2: High-throughput screening technologie: het gebruik van adenovirale collecties om
menselijke cellen te screenen.
Eiwitten worden ingedeeld in verschillende klassen op basis van hun werking en structuur.
Onderzoekers in de farmaceutische industrie zijn het er in het algemeen over eens dat
bepaalde klassen eiwitten beter reageren op medicijnen dan andere klassen. Deze eiwitklassen
worden “drugable” genoemd en vormen de basis van de meeste onderzoeksprogramma’s
naar medicijnen. Galapagos heeft een gerichte collectie van virussen opgebouwd die zorgen
voor hetzij een knock-in (FLeXSelect®), hetzij een knock-down (SilenceSelect®) van de
drugable eiwitten. Met deze collecties heeft Galapagos menselijke cellen gescreend die
betrokken zijn bij ziektes zoals osteoartritis, osteoporose en reumatoïde artritis en eiwitten
geïdentificeerd die deze ziekten controleren. Door deze eiwitten vervolgens verder te testen
(valideren) in meer geavanceerde studies, heeft Galapagos een aantal targets gevonden voor
de ontwikkeling van nieuwe medicijnen.
Op basis van de targets die met deze technologie ontdekt zijn, is Galapagos momenteel drug
discovery onderzoek aan het doen. Wanneer eenmaal een target gevalideerd is, wordt het
getest tegen grote collecties van chemische kleine moleculen om structuren te identificeren
die een interactie hebben (blokkering / activering) met het target. Deze chemische structuren
worden vervolgens geoptimaliseerd om “medicijn-eigen” karakteristieken te verkrijgen,
waarna het kandidaat-geneesmiddel in de kliniek verder getest wordt, Dit proces van het
ontdekken van geneesmiddelen is vergelijkbaar met de aanpak van grote farmaceutische
bedrijven en heeft geresulteerd in breakthrough geneesmiddelen zoals Gleevec®, van
recentelijk goedgekeurd oncologieproduct van Novartis.
Het onderscheidend vermogen van Galapagos ligt in het gebruik van menselijke cellen,
hetgeen een meer realistisch beeld geeft van het effect dat een eiwit kan hebben op de ziekte
in het menselijk lichaam dan het bestuderen van eiwitten in aangepaste cellen (cellijnen) en
dierlijke cellen, zoals door andere ondernemingen wordt toegepast. Bovendien richt Galapagos
zijn inspanningen op de drugable eiwitten en kan zij deze eiwitten efficiënt screenen in
menselijke cellen. Galapagos gelooft dat deze unieke aanpak om targets te identificeren en te
valideren de slagingskans vergroot om nieuwe medicijnen naar de markt te brengen.
Naast dat de adenovirale collecties en screening-technologieën de basis vormen voor
Galapagos’ interne target identificatieactiviteiten, worden deze ook ter beschikking gesteld aan
academische instituten en farmaceutische ondernemingen via BioFocus, een servicedivisie van
Galapagos. Vele partners hebben Galapagos’ technologie al toegepast in een aantal
ziektegebieden, waardoor het de wetenschappelijke en farmaceutische werelden helpt om de
oorzaken van ziektes beter te begrijpen en daarmee de ontwikkeling van nieuwe medicijnen te
bevorderen.