En de mens
schiep leven
Niet langer zijn door de natuur gevormde wezens de enige
levensvormen op aarde. Vorige maand presenteerden
Amerikaanse onderzoekers ’s werelds eerste synthetische
levensvorm, een bacterie met DNA dat ze chemisch in elkaar
hadden gezet. Welke wonderlijke weg is de wetenschap
eigenlijk ingeslagen? Door Hidde Boersma • Illustratie Merel Haasnoot
nwtmagazine |
21
Leven in de brouwerij: om synthetisch
leven te maken, liet het team van Venter het
meeste werk uitvoeren door heel gewone
bacteriën en gistcellen, zoals deze kolonie in
een petrischaaltje. Foto: Shutterstock
H
oe raar kan het lopen.
3,5 miljard jaar lang was het
huidige leven het enige dat
leefde op deze planeet. Alles
stamde af van één voorouder,
van een paar gebeurtenissen in een warme
modderpoel, zoals Darwin aannam. Totdat
een stel wetenschappers leven maakten.
Zomaar, door een serie chemische onderdelen in het lab bij elkaar te stoppen. Opeens lopen er twee levensvormen en twee
evoluties langs elkaar heen, en die tweede
levensvorm valt te sturen. We kunnen het
laten uitvoeren wat we willen: de olievlek
voor de Amerikaanse kust opruimen, de
accu van een auto vervangen, of de nieuwste kankermedicijnen produceren.
Fantasie? Niet lang meer. Eind mei
maakten Amerikaanse wetenschappers
bekend dat ze er voor het eerst in geslaagd
waren om een synthetische levensvorm te
maken (Science, 21 mei 2010). Synthia, zo
wordt ’s werelds eerste kunstmatige
organisme genoemd. Eerlijk is eerlijk, zo
heel synthetisch is Synthia nu ook weer
niet. De bacterie waarom het gaat – want
dat is het – bestaat vooral uit gewone,
organische bouwstenen en is deels gemaakt van een al bestaande bacterie. Het
betreft dus eerder een microscopisch monster van Frankenstein dan om een werkelijk nieuw wezen: in feite kregen de onderzoekers een al bestaande bacterie aan de
praat door er een chemisch vervaardigde
sliert DNA in te stoppen. Maar raar is het
toch ook weer wel. En nu de geest eenmaal
uit de fles is, zal er meer volgen.
Lang leek het de normaalste zaak dat er
uit niet-levend materiaal leven kon ontstaan. Tot diep in de 19e eeuw was de
theorie van spontane generatie, ooit beschreven door Aristoteles, gemeengoed.
Zo’n 350 jaar voor Christus beschreef de
Griekse filosoof in zijn boek Geschiedenis
van de dieren dat, hoewel sommige dieren
voortkomen uit ouders van dezelfde soort,
andere spontaan ontstonden. Bewijzen
hiervoor zag hij in het ontstaan van insecten
uit verrotte groente en het verschijnen van
maden in de ingewanden van dode dieren.
Ondanks de tegenstelling met het
verhaal in het Bijbelboek Genesis, haakten
Christenen aan bij de theorie en zo overleefde generatio spontanea zonder veel
tegenstand de Middeleeuwen. Pas in 1669
kwamen de eerste barsten in de theorie: de
Italiaanse wetenschapper Francisco Redi
ontkrachtte het idee dat maden zomaar
ontstonden uit rottend vlees, door potten
afgedekt en onafgedekt vlees met elkaar te
vergelijken: de afgedekte potten bleven
verschoond van de wormpjes. Maar pas
toen Louis Pasteur in 1859 aantoonde dat
ook bacteriën niet konden ontstaan in een
afgedekt steriel voedingsmedium, was de
theorie voorgoed verleden tijd.
100 µm
De eerste door een synthetisch genoom
bestuurde bacterie, met de machineachtige naam
M. mycoides JCVI-syn 1.0, slaat blauw uit ten
teken dat het synthetische genoom werkt. De
genen van de bacterie laten een stof waarin de
bacterie leeft blauw uitslaan. foto: Science/AAAS
De ontdekking van Pasteur leek een duidelijke scheidslijn af te bakenen tussen
levende en niet-levende natuur. Leven komt
voort uit leven, en niet-levend materiaal kan
op geen enkele manier tot leven worden
gewekt. Levend materiaal had een bepaalde
levenskracht in zich, vis vitalis, die niet was
weggelegd voor niet-levend materiaal.
Maar ondertussen was in Duitsland die
strikte scheiding alweer tenietgedaan.
Leven maken doe je zo
Zelf ook eens knutselen met
leven? Wat het dichtst in de
buurt komt is misschien nog
wel de jaarlijkse international
Genetically Engineered Machine
(iGEM)-competitie van het
Massachusetts Institute of
Technology (MIT). Studenten
die eraan deelnemen kunnen
vrijuit ‘BioBricks’ bestellen op
internet (biobricks.org/),
stukken DNA met daarop
genen en schakelaars om die
genen te reguleren. Vervolgens
krijgen ze een map opgestuurd
met daarin uitdrukbare papier-
22
tjes waarop het bestelde stuk
DNA is gedroogd. Dat kunnen
ze vervolgens inbouwen in
bijvoorbeeld de standaard
laboratoriumbacterie E. coli en
het zo op allerhande manieren
aanpassen.
Sinds 2007 doen er aan de
competitie ook teams uit de
Lage Landen mee, van onder
meer de TU Delft en de Rijksuniversiteit Groningen. Nog
vorig jaar behaalde het Groningse team een gouden
medaille met een bacterie die
zo was omgebouwd dat hij
| nwtmagazine | juli/augustus 2010
Blokkendoos: aan het Massachusetts Institute of Technology
toont synthetisch-bioloog Drew
Endy flesjes met daarin ‘Biobricks’: stukjes kant en klaar
synthetisch DNA die als bouwstenen worden gebruikt bij de
vervaardiging van genetisch
aangepaste cellen. foto: SPL/ANP
zware metalen uit verontreinigd
water opneemt. Het organisme
produceerde vervolgens ook
nog eens luchtblaasjes, waardoor het kwam bovendrijven en
makkelijk is te verwijderen. In
2007 behaalde Delft dezelfde
medaille, met een bacterie die
de suiker xylose uit gewasresten omzet in bio-ethanol.
De laatste editie mocht
overigens rekenen op de
belangstelling van de FBI, die
kennis wil opdoen over de
gevaren van synthetisch
biologie.
Chemicus Friedrich Wöhler slaagde er in
1828 namelijk in om ureum te synthetiseren, een organische stof waarvan men
dacht dat die alleen door levende organismen kon worden geproduceerd. Wöhler
maakte het echter uit zilverisocyanaat en
ammoniumchloride, twee anorganische,
niet levende stoffen.
Met Wöhlers ontdekking was het startschot voor de zoektocht naar synthetisch
leven gegeven. Als we organische moleculen kunnen synthetiseren, dan moeten we
ook het hele leven kunnen nabootsen, zo
was de gedachte.
De honderd jaar daarop boekte men
echter weinig vooruitgang. Natuurlijk was
er het fameuze Urey-Miller-experiment,
waarbij uit simpele moleculen spontaan
aminozuren, de bouwstenen van eiwitten,
ontstonden. Maar echt dichtbij leven
kwam het niet. Pas toen men in de jaren
zestig en zeventig met moleculaire methoden inzicht kreeg in de werking van onze
elementaire bouwstenen – DNA, RNA en
eiwitten – kwam er vaart in het project.
Vooral de laatste twintig jaar zijn meerdere vooraanstaande vakgroepen bezig om
als eerste een organisme te maken dat
volledig door de mens is gemaakt. Denk
niet gelijk aan een koe of een boom; de
focus ligt vooral op microscopisch leven,
bijvoorbeeld op bacteriën. Dat is niet alleen
relatief gemakkelijker om te maken,
bacteriën komen ook sneller van pas.
Bacteriën zijn namelijk als geen ander in
staat om voor ons nuttige processen uit te
voeren, van medicijnen produceren en
vervuilende stoffen afbreken tot het aanmaken van milieuvriendelijke brandstof.
Zeker, veel van dat soort toepassingen
kun je ook op een chemische of mechanische manier bereiken, maar beide zijn
vaak energierovend en erg inefficiënt. Het
Tot diep in de 19e eeuw
dacht men dat er uit
niet-levend materiaal
leven kan ontstaan
leven heeft met zijn waaier aan enzymen
veelal de meest efficiënte manier gevonden voor dit soort processen. Bovendien is
leven in staat zichzelf te kopiëren, waardoor het reacties oneindig lang kan uitvoeren. Vaak heeft het daar bovendien alleen
maar een paar simpele voedingsstoffen
voor nodig. Gemakkelijker en sneller dan
dat wordt het niet.
Leven maken, ga er maar aan staan. Bacteriën zijn dan misschien simpele wezens,
daarmee is niet gezegd dat ze gemakkelijk
zijn na te maken. Ze zijn nog steeds
ingewikkelde creaties, waar miljarden
jaren evolutie overheen is gegaan. De
hoeveelheid eiwitten, DNA en andere
moleculen in één bacteriële cel is enorm.
Vandaar dat nogal wat wetenschappers
besloten eerst maar eens een stap terug te
doen, naar het meeste basale leven, om
van daaruit de zoektocht naar synthetisch
leven te beginnen.
De huidige pogingen om leven te
creëren vallen ruwweg te verdelen in twee
strategieën. De eerste beweging probeert
het minimale huidige leven op te sporen
om dat vervolgens na te maken: de topdownmethode. De tweede groep wetenschappers probeert ‘van onderaf’ leven te
creëren. Met zo simpel mogelijke bouwblokken proberen ze protocellen te maken,
die kunnen delen en evolueren.
De eerste route lijkt vooralsnog de
meeste aandacht te krijgen, vooral omdat
de mediagenieke Amerikaanse wetenschapper Craig Venter tot die beweging
hoort. Venter, verbonden aan het Institute
for Genomic Research in Rockville en
vooral bekend als diegene die als eerste
erin slaagde om de basenvolgorde van het
DNA van de mens te ontrafelen, begon
vijftien jaar geleden met zijn missie om een
genoom na te maken in het laboratorium.
Dat deed hij met een zogeheten DNA-synthesizer, in feite een apparaat met vier
verschillende flessen, elk gevuld met de
juli/augustus 2010 | nwtmagazine |
23
letters – basen – waaruit onze levenscode
bestaat: A, C, G en T. De synthesizer ‘rijgt’
die in de gewenste volgorde aan elkaar.
Om het niet te moeilijk te maken, begon
Venter met het kleinst bekende genoom
waarvan wetenschappers het bestaan
kennen, dat van Mycoplasma genitalium.
Deze parasiet, die leeft in het voortplantings- en ademhalingssysteem van primaten, bezit maar 470 genen en heeft een
grootte van ongeveer 580.000 basenparen.
Hij kan met een relatief klein genoom toe,
omdat hij uitgebreid teert op door zijn
gastheer geproduceerde voedingsstoffen.
Het lijkt zo gemakkelijk, DNA synthetiseren; een druk op de knop en het gewenste
DNA rolt uit de synthesizer. Toch zijn de
apparaten die wetenschappers tot nu toe
gebruiken om de onderdelen van het DNA
aaneen te rijgen nog notoir onbetrouwbaar
en langzaam. De chemische reacties die ten
grondslag liggen aan het aan elkaar zetten
van de basen, zijn omslachtig en moeilijk te
controleren. De reactie mislukt regelmatig,
met als gevolg dat er een verkeerde DNAvolgorde uit het apparaat rolt. Dat betekent
dat men elk gemaakt stuk moet controleren
en soms herstellen. Het is daarom alleen
efficiënt om kleine stukken te maken, daar
de goed gelukte uit te kiezen en die vervolgens aan elkaar te lijmen – monnikenwerk.
Het grootste stuk DNA dat Venters team
na jaren ploeteren met deze techniek wist
te construeren, was dat van het poliovirus
(Science, 11 juli 2002). Dat heeft echter
maar 7000 basenparen, een fractie van het
aantal basenparen van het kleinste bacte-
riegenoom. En virussen gelden niet als
synthetisch leven: een virus staat namelijk
niet als levend te boek, omdat ze zich alleen
met behulp van een gastheer staande
kunnen houden. Er leek geen beginnen aan
om met deze techniek een volledig bacterieel genoom te synthetiseren.
Gelukkig voor Venter werd het aflezen
van DNA-codes de laatste jaren steeds
gemakkelijker en goedkoper (zie ook
NWT, september 2009). Tegenwoordig
kunnen wetenschappers de volledige
DNA-volgorde van een mens in één nacht
bepalen. De controlestap gaat daarom
De DNA-synthesizer
rijgt de bouwstenen
van de levenscode in
volgorde aan elkaar
steeds sneller: het is nu mogelijk om
duizenden kleine gesynthetiseerde stukken razendsnel te controleren en de goede
eruit te pikken.
Het probleem is nog wel dat je vervolgens zit met talloze kleine onderdelen, die
allemaal achter elkaar moeten worden
gezet. Kleine stukken, tot ongeveer duizend basenparen, kun je nog in reageerbuisjes aan elkaar plakken. Daarna doemt
echter een nieuw probleem op: langere
stukken raken in de knoop.
‘Synthia’ door de microscoop, gevriesdroogd.
‘Synthia’ tijdens de celdeling.
foto: Science/AAAS
foto: Science/AAAS
24
| nwtmagazine | juli/augustus 2010
Om de iets grotere stukken toch aan elkaar
te lijmen, moest Venter een list verzinnen.
Hij besloot uit te wijken naar een bacterie.
De gebruikte bacterie, het laboratoriumwerkpaard E. coli, slaagde er al in om
langere stukken aan elkaar te zetten, maar
bleek er bij stukken van zo’n honderdduizend basenparen ineens mee op te houden. Een korte zoektocht volgde, en uiteindelijk bleek het simpele bakkersgist wel in
staat om grote stukken te combineren tot
één streng. Bovendien is de gist in staat om
de aan elkaar geregen delen te kopiëren. Zo
hoefde Venter niet steeds uit te wijken naar
het matig werkende DNA-synthese-apparaat, maar kon hij de natuur een deel van
het werk laten doen.
Maar daar kwam alweer het volgende
probleem om de hoek kijken. Bacteriën en
gisten zijn zo totaal verschillend van elkaar,
dat er genetische gist-signalen in de strengen
van het synthetisch bacterie-DNA moesten
worden ingebouwd, om het kopiëren te
laten werken. Ook daar slaagde Venter
uiteindelijk in. In 2008 lukte het hem dan
toch eindelijk de eerste synthetische versie
van het DNA van Mycobacterium genitalium
te maken (Science, 29 februari 2008).
Kaping
Daarmee was echter alleen nog maar de
genetische ‘software’ voor een synthetische
cel aanwezig. Een lang stuk informatie,
meer is zo’n genoom niet – software zonder
hardware. Hoe laat je de software zijn eigen
hardware maken, oftewel een cel?
Venter zocht de oplossing in, zoals hij
het zelf noemde, genetische alchemie. Hij
besloot het zelfgemaakte DNA in te brengen in een donorcel, waar de synthetische
variant het oorspronkelijke DNA vervolgens moest wegconcurreren. Een soort
kaping van een cel, dus.
Om het principe te testen, probeerde
Venter het eerst uit met bestaand, biologisch DNA. Hij isoleerde hiervoor DNA uit
cellen van de bacterie Mycoplasma mycoidis en plaatste dat vervolgens in een
andere bacterie, Mycoplasma capricolum.
Beide soorten zijn familieleden van
Mycoplasma genitalium, hebben een net
zo klein genoom, maar groeien sneller en
zijn dus gemakkelijker om mee te werken.
Vorig najaar was het eindelijk zo ver:
Venter slaagde er toen in om met een
zogenoemde genoomtransplantatie van
Craig Venter: “Synthetisch leven is nu een soort, onderdeel
van de inventaris van de aarde.” foto: Hollandse Hoogte
de ene bacteriesoort een andere soort te
maken, iets wat lang niet voor mogelijk
werd gehouden (Science, 3 augustus 2009).
Maar ook deze stap op weg naar Synthia
had heel wat voeten in de aarde. Bacteriën
hebben van nature een systeem waarmee
ze vreemd DNA herkennen en kapot
knippen, een beetje vergelijkbaar met hoe
ons immuunsysteem lichaamsvreemd
materiaal herkent. Bacteriën gebruiken
daarvoor speciale eiwitten, de zogeheten
‘restrictie-enzymen’. Die maken het DNA
op zeer specifieke plaatsen kapot. Dus
moest Venter, voordat hij het donor-DNA in
de ontvangende cel kon stoppen, eerst al
die potentiële knipplaatsen beschermen.
Dat kan door met een specifiek enzym er
een bepaalde chemische verbinding aan te
hangen, een proces dat methylering heet.
Het getob met de restrictie-enzymen
bezorgde Venters team echter ook een
goede ingeving. De onderzoekers besloten
aan het donorgenoom speciale genen toe te
voegen die coderen voor specifieke restrictie-enzymen die het originele DNA van de
gastheer herkennen. De bacterie Mycoplasma capricolum zal niet hebben geweten wat
hem overkwam: opeens kwam daar een
sliert DNA aan die niet alleen gepantserd
Als een levend stoplicht lichten genetisch
veranderde bacteriën op in een petrischaaltje. De microben bestaan uit ‘zenders’ (midden) die met chemische signaaltjes de omliggende bacteriën gekleurd laten oplichten.
Dergelijke systemen kunnen een rol spelen
als sensor of als diagnose-apparaat bij ziekten. Hoe ‘synthetischer’ de bacteriën, des te
controleerbaarder dergelijke systemen zijn.
foto: SPL/ANP
was tegen de restrictie-enzymen van M.
capricolum zelf, maar die ook nog eens zélf
restrictie-enzymen afvuurde, bedoeld om
M. capricolums DNA te verwoesten. Een
soort DNA-tank, die de cel kon overnemen
door het oude DNA te verwoesten.
Om zeker te weten dat de transplantatie
was gelukt, had Venter aan het donor-DNA
ook nog een gen toegevoegd die ervoor
zorgt dat de bacterie blauw wordt als het
gen – en dus het genoom – aanstaat. Een
soort overwinningsvlag, eigenlijk. En
inderdaad verschenen op een groeimedium in het laboratorium na verloop van tijd
DNA 2.0
De natuur en de evolutie
verslaan in hun eigen
ingenieuze concepten, ook
dat is synthetische biologie. Jason Chin, onderzoeker aan de universiteit van
Cambridge is zo iemand
die dat doet: hij is erin
geslaagd om de genetische
code van het DNA volledig
te herinterpreteren en zo
eiwitten te maken met
daarin aminozuren die
cellen normaliter niet
gebruiken (Nature, 18
maart 2010).
In al het leven wordt de
genetische code afgelezen
in ‘triplets’: drie letters
coderen voor één type
26
aminozuur. Het ribosoom
(de eiwitfabriek van de
cel) rijgt bijvoorbeeld het
aminozuur proline aan
een eiwit als het triplet
CCA tegenkomt. In totaal
zijn er 64 combinaties
mogelijk die voor 20
verschillende aminozuren
coderen.
Chin heeft het ribosoom
echter zo aangepast, dat
het vierletterige codes kan
lezen. Met die nieuwe
mogelijkheid kan een
ribosoom aminozuren
inbouwen die niet in het
standaardrepertoire van
20 aminozuren zitten. Dat
levert in theorie 256
| nwtmagazine | juli/augustus 2010
mogelijkheden voor
aminozuren op, in plaats
van 64. Tot dusver is Chin
zelf overigens niet verder
gekomen dan het aangepaste ribosoom één nieuw
type aminozuur te laten
inbouwen.
Dat nieuwe type aminozuur zorgt voor extra
stabilisatie van eiwitten.
Handig voor eiwitten die
onderhevig zijn aan sterke
krachten of hoge temperaturen, zoals die in wasmiddelen, meent Chin. Opvulling van de overige 255
plaatsen moet leiden tot
eiwitten met een waaier
aan nieuwe functies.
blauwe kolonies: de eerste DNA-transplantatie ooit was gelukt, en misschien nog wel
bijzonderder, van één soort bacterie was
een ander gemaakt.
Logischerwijs volgde Venter daarna
dezelfde procedure voor zijn synthetische
genoom. Negen maanden later was de
geboorte van de eerste cel die draait op
kunstmatige genetische software een feit
(Science, 20 mei 2010). “Venter maakt leven
in het lab”, klonken de nieuwskoppen. “Een
keerpunt in de geschiedenis van de biologie en de biotechnologie”, commentarieerde de Amerikaanse filosoof Mark Bedau in
Nature. “Venter wrikt de meest diepzinnige
deur in de geschiedenis van de mensheid
open, en werpt misschien wel een blik op
onze lotsbestemming”, verklaarde de
Roemeens-Australische ethiekhoogleraar
Julian Savulescu, een autoriteit op het
gebied van biotechnologische ethiek. “Hij
is het leven niet kunstmatig aan het kopiëren of aan het veranderen. Hij beweegt zich
richting de rol van God: leven scheppen dat
van nature nooit had kunnen bestaan.”
Venter zelf liet zich intussen in niet minder
grootse woorden uit. “Het is nu een levende
soort, onderdeel van de inventaris van de
aarde”, zei hij tegen Science.
Maar niet iedereen is het daarmee eens.
“Om het genoom aan te schakelen en de
cel in werking te zetten, gebruikt hij nog
steeds de eiwitten van de originele cel. Die
zijn allesbehalve synthetisch”, verduidelijkt
Roel Bovenberg, hoogleraar synthetische
biologie aan de Rijksuniversiteit Groningen en biotechnoloog bij voedingsmiddelenconcern DSM. “Je zult al die eiwitten in
het laboratorium moeten maken, om er
echt door de mens gemaakt leven van te
maken. Dat zijn er echter zoveel, dat zie ik
de eerste tien jaar nog niet gebeuren.”
Eiwit
Kunstmatige eiwitten, dus. George Church,
hoogleraar genetica aan Harvard Medical
School, is daar in ieder geval al een tijdje
mee bezig. Hij richt zich daarbij op het
ribosoom, het enzym dat verantwoordelijk
is voor de productie van eiwitten in een cel.
Het ribosoom is een van de meest essentiële onderdelen van het leven zoals wij dat
kennen. Al het leven op aarde bezit ribosomen, die er bovendien in alle koninkrijken
van het leven bijna identiek uit zien. Dat
maakt het aannemelijk dat de eiwitfabriek
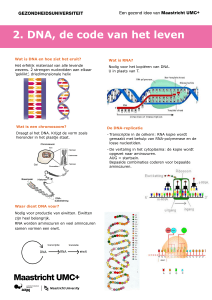
Tekst M. Keulemans, naar ETC Group.
Tekening Stig. www.etcgroup.org
Om een synthetische levensvorm te verkrijgen,
moet je eerst zijn DNA maken. Synthetisch DNA
(sDNA) wordt gemaakt in een zogenoemde
DNA-synthesizer. Dat apparaat bevat een
computer die kan worden geprogrammeerd om
welke DNA-volgorde dan ook te maken.
Het vergt een reeks chemische reacties om een
molecuul DNA te ‘kweken’. De DNA-synthesizer
dient de chemische ingrediënten daarvoor in de
juiste volgorde toe. Makkelijker gezegd dan gedaan:
alleen al een bacterie vereist een zeer lange DNAstreng. In een menselijke cel komen de ‘letters’
A, G, C en T drie miljard keer voor!
Mycoplasma
genitalium
Vandaar dat de meeste wetenschappers die
synthetisch leven willen maken een kortere
route nemen: ze bestellen hun sDNA op internet
van zogenoemde ‘foundries’, bedrijven die stukken
synthetisch DNA maken zoals een fabriek autoonderdelen maakt. Om een synthetisch organisme
te maken, zul je zijn hele DNA-volgorde nodig
hebben: een genoom.
Craig Venter, CEO en oprichter van Synthetic
Genomics, maakt bovendien gebruik van bacteriën
en gistcellen. Die zorgen ervoor dat de langere
stukken synthetisch DNA aan elkaar worden gezet.
Venter maakt echter niet hele cellen, maar
alleen het DNA in de cel. Als uitgangspunt
nam het team van Venter een bacterie die al
bestaat, Mycoplasma genitalium. Deze bacterie
heeft een erg klein genoom.
De wetenschappers verwijderden stukken van
M. genitalium’s DNA, maar niet genoeg om hem
te doden. Ze noemen dit uitgeklede DNA het
‘minimale’ genoom. Vervolgens maakten ze het
na van synthetisch DNA.
Daarna ‘wapenden’ ze het synthetische DNA om
te voorkomen dat het zou worden afgebroken en
injecteerden ze het in de bacterie. Daar wist het
zich te vestigen. De cellen begonnen te delen,
met in hun binnenste een door mensenhanden
gemaakt genoom.
En ziedaar: een synthetische levensvorm is
geboren! Zoals alle levensvormen, moet Venters
synthetische organisme kunnen delen en muteren.
En volgens critici kan dat wel eens het begin zijn
van allerlei problemen...
een van de vroegst ontwikkelde eiwitten
was toen het leven op aarde begon. Kennis
van de synthese van dit enzym raakt
daarom aan de basis van het leven zelf, en
zou bovendien de productie van een veel
simpelere synthetische cel dichterbij
kunnen brengen, besefte Church.
Church slaagde in zijn missie door een
bestaand ribosoom af te breken en die
weer spontaan op te laten bouwen. Zoiets
was al eens gelukt aan het eind van de
jaren zestig, maar toen in extreme omstandigheden die niet overeenkwamen met
hoe het leven ooit is begonnen. Bovendien
zouden die omstandigheden niet rendabel
zijn voor industriële toepassingen van
synthetisch leven. Het ribosoom dat
Church synthetisch bouwde, bleek goed in
staat om luciferase, het lichtgevende eiwit
van de vuurvlieg, zo in elkaar te zetten dat
het werkte en dus licht gaf.
In veel wetenschappelijke media beweert Church dat hiermee het maken van
leven louter een kwestie is van geld en tijd.
Immers: nu we DNA en eiwitten kunnen
synthetiseren, is het in theorie alleen nog
maar een kwestie van de boel combineren.
“Met 10 miljoen dollar moet het lukken om
het minimale genoom en de eiwitten die
ervoor nodig zijn om het systeem op te
starten, te produceren”, zo liet Church
optekenen in het Britse blad New Scientist.
“Toch is het raar dat er nog geen publicatie in een erkend, peer-reviewed vakblad
is verschenen over de ribosoomvinding”,
stelt Bovenberg daarentegen. Zo is nog
altijd niet in detail bekend wat dan die
‘normale omstandigheden’ waren waaronder Church zijn ribosoom aan de praat
kreeg. Bovenberg: “Church is een betrouwbare wetenschapper, en ik vertrouw erop
dat de publicatie wel komt, maar het is
toch alweer een jaar geleden dat hij deze
vinding heeft aangekondigd op congressen. De manier waarop hij het voor elkaar
juli/augustus 2010 | nwtmagazine |
27
Synthe­tisch-levenmaker George Church, poserend bij een
DNA-synthesizer: “Met 10 miljoen dollar moet het mogelijk zijn
leven uit het niets te maken.” foto: SPL/ANP
heeft gekregen, blijft op dit moment een
beetje vaag en oncontroleerbaar.”
“Bovendien”, zo stelt Bert Poolman, ook
hoogleraar synthetische biologie aan de
Rijksuniversiteit Groningen, “is het aanzetten van een minimale cel veel meer dan
een genoom en wat eiwitten in een blaasje
stoppen en vervolgens afwachten. Regulatie in een cel verloopt zo nauwkeurig, daar
weten we nog maar bar weinig van.”
Energie
Ze zijn dus aardig op weg, die top-downwetenschappers, maar echt volledig synthetisch leven is het nog niet. Zou de aanpak
van onderaf, dus onderdeel voor onderdeel,
sneller gaan? Voorwaarde is dat het lukt om
iets te creëren dat voldoet aan de drie criteria
van leven: voortplanting op basis van een
erfelijkheidsdrager, een stofwisseling
inclusief het opvangen van energie, en iets
dat op een cel lijkt – een afgesloten ruimte.
Een heel gepuzzel nog, leven maken uit
het niets. Toch lukt het wetenschappers in
verschillende laboratoria al heel aardig om
diverse losse stapjes te zetten: de een heeft
een werkend celwandje, de ander een zich
voortplantend sliertje erfelijk materiaal.
Een kunstmatig celmembraan lijkt het
gemakkelijkst. Al decennia is bekend dat
vetzuren, die een onderdeel van de celmembraan vormen, spontaan blaasjes
kunnen vormen. In een waterige oplossing
vormen ze bolvormige afgesloten ruimtes –
denk aan de kringen in een pan water met
olie erin – en een primitieve cel is daar.
De Italiaanse hoogleraar synthetische
biologie Pier Luigi Luisi maakt handig
gebruik van het zelfassemblerende vermogen van vetzuren. Hij voegde 36 enzymen
die allemaal betrokken zijn bij de aanmaak
van een groenfluorescerend eiwit toe aan
een reageerbuis met vetzuren tegen de
zijkant geplakt. Luisi lukte het om de
blaasjes de 36 eiwitten te laten inkapselen
en zo een soort cel te creëren die groen
oplichtte.
In een vervolgexperiment slaagde Luisi
er zelfs in om een klein stukje DNA in te
vangen, samen met enkele eiwitten die het
DNA konden aflezen. De genen op het
DNA waren verantwoordelijk voor de
aanmaak van vetzuren voor in de membraan, die zo van binnen werd uitgevoed
(Biochemical and Biophysical Research
Communications, 9 november 2007). Met
28
| nwtmagazine | juli/augustus 2010
Kunstmatige cellen? Vetzuren vormen
spontaan stabiele bolletjes in een waterige
oplossing. Diverse onderzoekers proberen in
de blaasjes onderdelen aan te brengen die van
de blaasjes een cel kunnen maken. Foto: SPL/ANP
wat schudden zouden de groter wordende
blaasjes uiteindelijk in tweeën kunnen
vallen, waarmee een primitieve vorm van
celdeling een feit is.
Het project van Luisi zit op het randje van
leven. De genen zijn synthetisch; de eiwitten niet, maar zouden dat kunnen zijn. Het
enige probleem is dat het DNA zich nog niet
kan kopiëren, zodat er geen echte celdeling
“Van de regulatie in
een cel weten we nog
maar bar weinig”
plaatsvindt. Het in tweeën vallen van de
blaasjes levert alleen maar een verdunning
op van de beginproducten. “Dat is waar we
nu staan”, constateert Poolman. “De meeste
onderdelen van leven kunnen we maken.
Maar het laten kopiëren van genetisch
materiaal lukt nog niet.”
Dat laatste is dan ook de focus van veel
onderzoek. En er zit enig schot in de zaak.
Nog vorig jaar lukte het onderzoekers
onder leiding van Gerald Joyce van het
Scripps Research Institute in de VS om
RNA te ontwikkelen dat zichzelf repliceert
(Science, 5 februari 2009). In een gewone
cel is RNA de boodschapper tussen DNA
en eiwitproductie, en vervult weinig meer
dan een tussenrol. RNA is echter zelf ook
drager van erfelijke informatie, en kan als
enzym fungeren dat een reactie katalyseert
– een rol die normaliter in een cel door
eiwitten wordt vervuld. Vandaar dat nogal
wat onderzoekers vermoeden dat RNA er
eerder was dan DNA: terwijl DNA zelf niets
‘doet’, is RNA behalve drager van erfelijke
informatie ook nog eens actief als enzym.
De groep van Joyce slaagde erin om een
systeem met twee RNA-enzymen te ontwikkelen die elkaar voortdurend optuigen.
Zo lang er maar een gelijkmatige toevoer is
van de afzonderlijke onderdelen van de
enzymen, kan het proces oneindig doorgaan. Het probleem is echter dat het
systeem nog erg ruw is, zoiets als een
werkende fotokopieermachine, maar
zonder dat er iets op de glasplaat ligt. Het is
namelijk nog niet gelukt om er een systeem van te maken met genetisch materiaal dat codeert voor stofwisseling of
membraanaanmaak. Er kan dus ook nog
geen echte evolutie plaatsvinden.
Ook Harvard-geneticus Jack Szostak, in
2009 winnaar van de Nobelprijs voor de
geneeskunde, bemoeit zich met de laatste
barrière. Zijn vakgroep houdt zich vooral
bezig met de vraag hoe het leven op aarde
is ontstaan. Zijn werk aan replicatie is
daarom erg fundamenteel. Net als Luisi
laat hij materiaal insluiten in zichzelf
vormende blaasjes en probeert daarbinnen replicatie op gang te krijgen.
Szostaks vorderingen zijn minimaal,
maar veelbelovend. De afgelopen jaren
slaagde hij erin om een klein stuk ‘opengeritst’, enkelstrengs DNA aan te vullen tot
het weer twee strengen had. In een cel
bestaat DNA normaliter uit twee strengen.
Als bij celdeling het DNA wordt gekopieerd, ontkoppelen de strengen en worden
bij beide enkele strengen nieuwe basen
ingebouwd, om zo verdubbeling tot stand
te brengen. De cel gebruikt daartoe een
hele sloot enzymen. Szostak lukte het om
binnenin een vetzuurblaasje een stukje
enkelstrengs DNA zónder hulp van enzymen aan te vullen tot dubbelstrengs DNA
(JACS, 16 september 2009).
Maar ook dat ging met kunst- en vliegwerk. Zo moest Szostak de DNA-bouwstenen, de basen, eerst chemisch aanpassen,
zodat ze niet met zichzelf gingen reageren.
Bovendien kwam hij niet verder dan een
stukje DNA met ongeveer twintig ingebouwde basen. Maar de positieve kant van het
verhaal is dat het ontstane dubbelstrengs
DNA weer enkelvoudig kan worden gemaakt door verhitting, waarna het inbouwen
weer opnieuw kan beginnen: een primitieve
vorm van replicatie is daar. Mocht Szostak
“Dit is geen monster
met het brein van een
psychopaat”
het enzymloos kopiëren uiteindelijk kunnen
optimaliseren, dan effent dat de weg naar
het maken van een simpelere cel.
Uiteindelijk zullen de Venters van boven
en de Luisi’s van onderaf elkaar ergens
halverwege tegenkomen, verwacht Poolman. “Van onderop lukt alleen de replicatie nog niet goed genoeg. En van bovenaf
hebben we nu wel een synthetisch stuk
DNA met replicerend vermogen, maar is
de rest van de celinhoud nog niet synthe-
tisch. Het is een kwestie van afwachten tot
we de tussenruimte begrijpen. Dan hebben we synthetisch leven.”
De toepassingen zullen nog wel even op
zich laten wachten, verwacht Bovenberg.
“De komende jaren zullen we vooral profijt
hebben van het aanpassen van bestaande
organismen, iets wat nu ook al op grote
schaal gebeurt,” stelt Bovenberg. “Bestaande
bacteriën hebben echter miljoenen jaren
evolutie ondergaan puur om te overleven, ze
zijn niet gemaakt voor industriële productie.
Zo gaat bijvoorbeeld bij medicijnproductie
dikwijls 90 procent biomassa verloren aan
bacteriële bijproducten, een inefficiënt en
duur grapje. Een synthetisch organisme dat
dat efficiënter kan, is zeer welkom.”
Dat is maar het begin. Experts zijn het
erover eens dat synthetisch leven op
termijn ongekende mogelijkheden biedt,
omdat het zo vrijelijk is in te richten. Een
soort steen der wijzen, die haast alle
denkbare taken kan verrichten.
Lastiger te overzien is de ethische kant.
Al direct na de bekendmaking van Venters
niet zo heel erg synthetische bacterie, klonk
er een roep om een onderzoeksstop, om na
te denken over de gevolgen. En uit een
peiling van de Wall Street Journal bleek dat
tweederde van de lezers meent dat alleen al
het besef dat er zoiets bestaat als kunstmatig leven op de een of andere manier zal
ingrijpen op zijn dagelijks leven.
Op zijn toonaangevende weblog over
evolutiebiologie Pharyngula is bioloog P.Z.
Meyers van de universiteit van Minnesota
genuanceerder. “Deze cel is geen monster
met tienmaal de kracht van een gewone cel
en het brein van een psychopaat”, schrijft
Meyers over de Venters cel. “Als de technieken verbeteren, zal iedereen gespecialiseerde bacteriën gaan bouwen om zeer
specifieke biochemische reacties te
verrichten. Ook dan zullen het slechte
generalisten zijn, die niet in staat zijn om te
concurreren met natuurlijke soorten.”
En op de langere termijn? “We hebben
geen idee wat onze kinderen en kleinkinderen hiermee kunnen doen. Ik denk niet
dat Wöhler (de chemicus die ureum synthetiseerde, red.) had kunnen voorzien dat zijn
ontdekking ooit tot plastics zou leiden. We
zullen moeten afwachten, genieten van de
rit, en goed bedacht moeten zijn op de
nieuwe beloften en gevaren die op ons
afkomen.” n
juli/augustus 2010 | nwtmagazine |
29