Krachtig
tegen Kahler
Een experimenteel medicijn tegen de ziekte multipel myeloom slaat boven
verwachting aan. Het middel werkt krachtig en heeft weinig bijwerkingen.
Dat blijkt uit een kleinschalige patiëntenstudie van het Erasmus MC.
Z
iekte van Kahler?
In Nederland staat multipel myeloom bekend als de
ziekte van Kahler. Hierbij woekeren de plasmacellen
- myeloomcellen - in het beenmerg, waar bloedcellen worden
aangemaakt. Dit tast het bot ernstig aan, zodat hevige pijn kan
ontstaan. Als gevolg van de botafbraak neemt bovendien de
hoeveelheid kalk (calcium) in het bloed sterk toe. Zo kunnen
de nieren beschadigd raken. Artsen stellen de ziekte van Kahler
elk jaar vast bij zo’n 800 volwassenen. Behandeling is een
expertise van het Erasmus MC.
Is Kahler te genezen?
In de afgelopen jaren is vooruitgang geboekt, maar deze ernstige aandoening is niet te genezen. De behandeling is zwaar en
na enkele jaren, doorgaans vier tot vijf, keert de ziekte meestal
terug. De patiënt moet dan opnieuw worden behandeld.
Waaruit bestaat de behandeling?
Vaak uit een combinatie van chemokuren en stamceltransplantatie van eigen stamcellen. In Nederland bevat de chemokuur
onder meer thalidomide (oude merknaam: Softenon) en
dexamethason. Een ander voorgeschreven middel is bortezomib (merknaam: Velcade).
Wat is het probleem?
Patiënten bij wie de voorgeschreven medicijnen falen, sterven
aan deze ziekte. Patiënten bij wie de behandeling wel aanslaat,
hebben het vaak moeilijk: de therapie is zwaar en de bijwerkingen zijn soms zo ernstig dat de behandeling voortijdig moet
worden afgebroken.
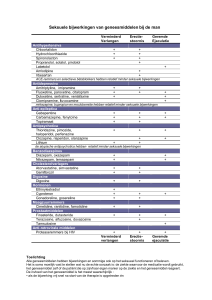
Wat zijn de bijwerkingen?
Patiënten kunnen onder meer een trombose oplopen. Er treedt
10
dan aderverstopping op als gevolg van thalidomide. Er is ook
perifere neuropathie mogelijk. Dit zijn vervelende en pijnlijke
zenuwaandoeningen aan de handen en voeten door toedoen
van bortezomib.
Wat doen hematologen?
Ze proberen in samenwerking met de neuroloog de neuro­
pathie met geneesmiddelen te behandelen, al moet soms ook
de bortezomib worden verminderd of gestaakt. Het Erasmus MC
onderzoekt of met genetisch onderzoek vooraf valt vast te
stellen hoe groot de kans is dat een patiënt de bijwerkingen zal
krijgen. Zo’n inschatting is mogelijk sinds het inzicht in de
genetica is gegroeid. Met de kennis uit het laboratorium proberen hematologen, ofwel ‘bloedziekteartsen’, een behandeling
op maat te maken, afgestemd op de individuele patiënt.
Wat heeft het Erasmus MC ontdekt?
De afdeling Hematologie van het Erasmus MC heeft als eerste
een experimenteel middel onderzocht bij vijftig volwassen
patiënten die net de diagnose multipel myeloom hadden
gekregen. Dit nieuwe middel - carfilzomib - werkt krachtiger
dan het bestaande bortezomib. Het heeft ook veel minder
bijwerkingen. De eerste indruk bij de kleine groep patiënten
is dat het medicijn ‘uitstekend’ werkt. Het middel kan worden
beschouwd als een doorontwikkeld, verbeterd ‘broertje’ van
bortezomib.
Wat heet ‘uitstekend’?
Prof. Pieter Sonneveld, hoofd Hematologie: “Bij 49 van de
vijftig patiënten die dit experimentele middel in het Erasmus
MC kregen, sloeg het medicijn goed aan, in combinatie met
thalidomide. Bij hen werd de ziekte 90% tot 100% verminderd.
Het middel bindt erg lang aan het eiwit dat het moet remmen
december 2011 • Monitor
Tekst Joop van de Leemput
Vermindering ziekte
en verrassend weinig
bijwerkingen
en kent daarnaast - een grote verrassing - weinig bijwerkingen.
Dit laatste is belangrijk, want dan kan de therapie worden
voortgezet. Eén van de vijftig patiënten moest voortijdig stoppen vanwege huidproblemen.”
Hij vervolgt: “Bijzonder aan de studie van het Erasmus MC is
dat wij die zelf hebben opgezet en dus ook de opzet en uitwerking van het onderzoek konden bepalen. Normaal gesproken
neemt de farmaceutische fabrikant het voortouw.”
Is het middel al verkrijgbaar?
Nee, het moet nog worden toegelaten door de keuringsinstanties van de overheid, zowel in de VS als in Europa. De verwachting is dat de positieve Rotterdamse resultaten zullen bijdragen
aan de toelating in 2012.
Verbeterd ‘broertje’ van
bestaand middel
Waaruit bestaat de nieuwe therapie?
Vier chemokuren met onder meer het nieuwe middel, die elk
een maand in beslag nemen, daarna een stamceltransplantatie
en tot slot weer vier chemokuren.
Wanneer komt dit middel beschikbaar?
In Nederland kan de patiënt dit nieuwe middel alleen in
studieverband krijgen, dus als iemand aan een wetenschappelijk onderzoek deelneemt. Het medicijndossier is
ingediend bij de EMA: de European Medicines Agency.
De verwachting is dat carfilzomib in de loop van 2012 wordt
toe­gelaten. Het is onmogelijk de exacte maand van toelating
te voorspellen.
Beeld Kirsten van Lom
Dit is de
druppel voor…
hoofd Genetisch Laboratorium
Inwendige Geneeskunde en bijzonder
hoogleraar Complexe Genetica van
Volksziekten André Uitterlinden
“Wat is de vruchtbare periode van een
vrouw? Wie krijgt osteoporose, ook wel
botarmoede genoemd? Wie houdt soepele
gewrichten? Hoe en waar wordt vet opgeslagen en voor welke ziekten is dat belangrijk op latere leeftijd? Sinds 2005 hebben
wij, vaak in grote internationale samenwerkingsverbanden, genen gevonden die een
rol spelen bij dit soort zaken.
Ieder mens is verschillend. Hij ziet er
anders uit en heeft zijn eigen specifieke
aanleg voor aandoeningen. Wij proberen
verbanden te leggen tussen enerzijds
verschillen in onder meer DNA van mensen
en anderzijds verschillen in hun uiterlijk of
ziekten. Het DNA halen we uit het bloed
van de onderzoekspersonen.
Het doel is tweeërlei. Allereerst behandeling. Onze kennis moet eraan bijdragen
dat we de biologie van allerlei ziekten
beter gaan begrijpen en er daarna middelen tegen kunnen worden ontwikkeld.
Daarmee zijn we bij het tweede streven:
diagnostiek. Als je op basis van iemands
genen weet voor welke ziekten hij aanleg
heeft en wanneer die zich gaan ontwikkelen, zou je actie kunnen ondernemen om
dat te voorkomen.
Dit alles staat nog in de kinderschoenen.
We hebben bijvoorbeeld al heel wat genen
gevonden die van betekenis zijn voor
diabetes type II en voor osteoporose,
maar hun afzonderlijke invloed is gering.
Je zou álle verantwoordelijke genen willen
kennen. Tot dusver hebben we nog slechts
een half procent van het DNA kunnen
analyseren. Graag zouden we met behulp
van een betere techniek - sequencen - de
volgorde van het hele DNA willen bepalen.
We hebben daartoe een subsidieaanvraag
ingediend bij de Nederlandse Organisatie
voor Wetenschappelijk Onderzoek.” (GS)