8
9
10
11
12
13
14
Allman FL. Fractures and ligamentous injuries of the clavicle and its
articulation. J Bone Joint Surg (Am) 1967;49:774-84.
Wilkins RM, Johnston RM. Ununited fractures of the clavicle.
J Bone Joint Surg (Am) 1983;65:773-8.
Neer 2d CS. Nonunion of the clavicle. JAMA 1960;172:1006-11.
Kay SP, Eckardt JJ. Brachial plexus palsy secondary to clavicular
nonunion. Case report and literature survey. Clin Orthop 1986;206:
219-22.
Leffert RD. Lesions of the brachial plexus, including thoracic outlet
syndrome. Instr Course Lect 1977;26:77-102.
Millesi H. Brachial plexus injuries. Management and results. Clin
Plast Surg 1984;11:115-20.
Sunderland S. Mechanisms of cervical nerve root avulsion in injuries
of the neck and shoulder. J Neurosurg 1974;41:705-14.
15
16
17
18
Medical Research Council. Aids to the investigation of the peripheral nervous system. Londen: Baillière Tindall; 1998.
Helm FCT van der, Pronk GM. Three-dimensional recording and
description of motions of the shoulder mechanism. J Biomech Eng
1995;117:27-40.
Rumball KM, Da Silva VF, Preston DN, Carruthers CC. Brachialplexus injury after clavicular fracture: case report and literature
review. Can J Surg 1991;34:264-6.
Della Santa D, Narakas A, Bonnard C. Late lesions of the brachial
plexus after fracture of the clavicle. Ann Chir Main Memb Super
1991;10:531-40.
Aanvaard op 16 juli 2001
Casuïstische mededelingen
Onbegrepen rechterventrikeldilatatie verklaard door een contusio cordis vele
jaren daarvoor
k.c.sybrandy, l.oosterom, c.burgersdijk en f.van der zant
Contusio cordis komt vaak voor in samenhang met een
stomp borstwandtrauma. Stompe borstwandtraumata
worden meestal veroorzaakt door verkeersongevallen.1
Histologisch wordt een contusio cordis gekenmerkt
door kneuzing van het hartspierweefsel. Afhankelijk
van de ernst van de beschadiging kan er een ruptuur van
de hartwand optreden, hetgeen kan leiden tot acuut
overlijden, of treedt er genezing op van de hartspier met
herstel van de cardiale functie.2 Herstel van een beschadigde hartspier kan gepaard gaan met een verandering
(‘remodeling’) van het ventrikel, gekenmerkt door dilatatie, vormverandering en compensatoire hypertrofie.3 4
In de volgende ziektegeschiedenis beschrijven wij een
patiënt van wie een onbegrepen rechterventrikeldilatatie en -hypertrofie slechts konden worden verklaard
door een doorgemaakte contusio cordis vele jaren daarvoor.
ziektegeschiedenis
Patiënt A, een 52-jarige man, werd door de huisarts naar de polikliniek Cardiologie verwezen met een sinds een halfjaar bestaande onregelmatige hartslag. Behalve dit bestonden er geen
belangrijke klachten. De cardiale voorgeschiedenis was blanco
en het cardiale risicoprofiel van patiënt was onbelast. Bij lichamelijk onderzoek werd een gezonde man gezien met een
normaal postuur. De bloeddruk bedroeg 120/80 mmHg, de
polsfrequentie was irregulair en rond de 80-90 slagen/min. Bij
auscultatie van hart en longen werden geen souffles of crepitaties gehoord. De lever was niet vergroot en er waren geen
oedemen. Het ECG toonde boezemfibrilleren met een rustige
ventrikelrespons van 85 slagen/min, een compleet rechterbundeltakblok, een intermediaire hartas en geen tekenen van
ischemie of doorgemaakt infarct. Op de thoraxfoto werd een
vooral rechtszijdig vergrote hartcontour gezien zonder afwijMedisch Centrum Alkmaar, Wilhelminalaan 12, 1815 JD Alkmaar.
Afd. Cardiologie: mw.K.C.Sybrandy (thans: Universitair Medisch Centrum, Utrecht) en mw.L.Oosterom, assistent-geneeskundigen; C.Burgersdijk, cardioloog.
Afd. Nucleaire Geneeskunde: F.van der Zant, nucleair geneeskundige.
Correspondentieadres: C.Burgersdijk.
samenvatting
Bij een 52-jarige man met nieuw ontstaan boezemfibrilleren
toonde transthoracale echocardiografie een geïsoleerd, aanzienlijk vergroot rechter ventrikel. Frequent voorkomende
oorzaken van rechterventrikeldilatatie werden uitgesloten.
Het beeldvormend onderzoek toonde een geïsoleerde dilatatie
van het ventraal gelegen deel van het hart, wat, in combinatie
met een stomp borsttrauma 30 jaar tevoren, een doorgemaakte contusio cordis deed vermoeden. Overeenkomstig hiermee
toonde myocardscintigrafie asymmetrische hypertrofie van de
rechterventrikelwand, die past bij ‘remodeling’ van de hartspier en die optreedt bij herstel na beschadiging. Na elektrische
cardioversie werd sinusritme verkregen; de patiënt bleef klachtenvrij.
kingen aan de longen. De lever-, nier- en schildklierfunctie
waren normaal.
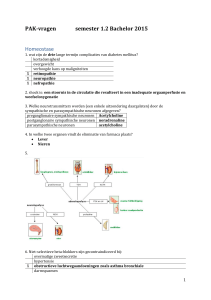
Het transthoracaal echocardiogram (TTE) liet een ernstige
dilatatie zien van het rechter ventrikel en rechter atrium met
een massale tricuspidalisinsufficiëntie (figuur 1). Aanwijzingen
voor pulmonale hypertensie, ziekte van Ebstein (misvorming
van de tricuspidalisklep) of een intracardiale shunt ontbraken.
De linker harthelft leek normaal. Er werd een ventilatieperfusiescan verricht, waarbij er geen aanwijzingen voor longembolieën werden gevonden. Tijdens het inspannings-ECG
was er een normale inspanningscapaciteit met een goede
bloeddrukopbouw en waren er geen angineuze klachten.
Een transoesofageale echo (TEE) bevestigde de enorme dilatatie van de rechter harthelft, de afwezigheid van een atriumseptumdefect (na contrastinspuiting) en toonde een gedilateerde tricuspidalisklepring en een normale structuur van de
tricuspidalis- en pulmonalisklep. De linker harthelft leek normaal.
Aangezien er op basis van deze onderzoeken nog geen aanknopingspunten voor de oorzaak van de enorm gedilateerde
rechter harthelft waren vastgesteld, werd een links- en rechtszijdige hartkatheterisatie uitgevoerd. Deze liet gave coronairen
zien (inclusief de rechterventrikeltak) en geen aanwijzingen
voor congenitale afwijkingen. De drukken die werden gemeten
(rechter atrium: gemiddeld 7 mmHg; rechter ventrikel: 16/2
mmHg; A. pulmonalis: 16/7 mmHg; pulmonale wiggendruk:
Ned Tijdschr Geneeskd 2001 15 december;145(50)
2443
rechter
ventrikel
linker
ventrikel
rechter
atrium
linker
atrium
figuur 1. Transthoracaal echocardiogram van patiënt A (horizontale doorsnede door de vier hartkamers): er is een enorme
dilatatie van het rechter ventrikel en het rechter atrium; het linker ventrikel en het linker atrium zijn normaal van grootte.
3 mmHg) waren normaal en er waren geen intracardiale shunts.
Het linker ventrikel contraheerde goed met uitzondering van
een klein apicaal aneurysma. Op een MRI kon geen vervetting
van myocardweefsel worden aangetoond, zodat aritmogene
rechterventrikeldysplasie niet waarschijnlijk was. Vanwege een
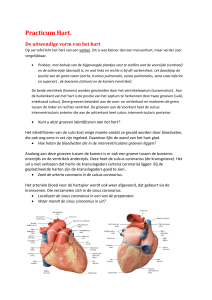
rechterbundeltakblokpatroon op het rust-ECG kon de diagnose ‘ischemie’ bij het inspannings-ECG niet met zekerheid worden uitgesloten en werd besloten tot een technetium-99m(99mTc)-sestamibi-inspanningsscintigrafie (figuur 2). Deze toonde geen ischemie of necrotische defecten, een normale linkerventrikelejectiefractie en een verdikte rechterventrikelwand.
De oorzaak van de enorme rechterventrikeldilatatie was dus
na uitgebreid onderzoek niet duidelijk. Bij een nieuwe afname
van de anamnese bleek patiënt 30 jaar geleden een motorongeval te hebben gehad, dat gepaard was gegaan met een stomp
borsttrauma, een leverruptuur en een clavicula- en onderbeenfractuur. Met dit nieuwe gegeven werden de TTE, TEE, het angiogram en de MRI opnieuw bekeken en werd vanwege de geisoleerde dilatatie van het ventraal gelegen deel van het hart,
namelijk het rechter ventrikel en de apex van het linker ventrikel, een doorgemaakte contusio cordis als waarschijnlijkste
diagnose beschouwd. In overeenstemming hiermee bleek ook
de hypertrofie van het rechter ventrikel bij 99mTc-sestamibiscintigrafie uitsluitend dorsaal gelokaliseerd, waardoor de
diagnose kon worden onderbouwd. In de tussentijd onderging
patiënt, na 6 weken antistollingbehandeling met acenocoumarol, elektrische cardioversie, waarbij het sinusritme herstelde.
Bij poliklinische controles nadien bleef de rechter harthelft
onveranderd gedilateerd, bleef het sinusritme behouden, was
patiënt klachtenvrij en behield hij een goede inspanningscapaciteit. Er traden geen tekenen van rechterventrikelfalen op.
2444
Ned Tijdschr Geneeskd 2001 15 december;145(50)
beschouwing
Contusio cordis wordt veroorzaakt door een stomp
borstwandtrauma en is meestal het gevolg van verkeersongevallen.1 5 Door plotse deceleratie slaat het hart, dat
in anteroposterieure richting relatief vrij kan bewegen,
tegen het borstbeen aan, maar ook kan myocardcontusie worden veroorzaakt door een uitwendige kracht direct op het borstbeen.2 In veel gevallen blijft een contusio cordis onopgemerkt, enerzijds door afwezigheid van
klachten of verwondingen aan de borstkas, anderzijds
door aanwezigheid van ernstige verwondingen waar alle
aandacht naar uitgaat.2 Vanwege concentratie op de
fracturen en de leverruptuur bij het motorongeval werd
waarschijnlijk ook bij patiënt A destijds de diagnose
‘contusio cordis’ niet gesteld.
Het herkennen van een acute contusio cordis is moeilijk. Lichamelijk onderzoek is onbetrouwbaar. Myocardcontusie kan hartkloppingen of lichte pijnklachten in de
borst geven, die, indien borstwandverwondingen voorkomen, vaak aan deze worden toegeschreven. Een röntgenfoto van de thorax dient enkel ter uitsluiting van
afwijkingen aan longen, vaatstructuren of het thoracaal
skelet. Het spierenzym creatinekinase (CK) is bij traumapatiënten altijd verhoogd en dus onbruikbaar voor
het aantonen van myocardschade. Myocardspecifiek CK
(CK-MB) kan de specificiteit voor hartspierschade verhogen, maar is bij hoge waarden van CK vaak foutpositief.1 2 Meting van troponine I, een molecuul dat al-
leen in hartspierweefsel voorkomt, bleek het geschiktst
om myocardschade aan te tonen bij multitraumapatiënten.6 Ook het ECG is weinig specifiek en kan normaal
zijn of kan ST-T-afwijkingen, Q-golven, (rechter)bundeltakblok of boezemfibrilleren laten zien.2 7 8
De diagnose wordt gesteld op basis van wandbewegingsstoornissen bij echocardiografisch onderzoek of
nucleair onderzoek. In eerste instantie kan een TTE
worden uitgevoerd; bij ernstig borstwandtrauma of
moeilijk te interpreteren TTE-beelden wordt een TEE
aanbevolen.1 2 7 Myocardcontusio gaat in de acute fase
gepaard met een verminderde ventrikelfunctie, die in
de meeste gevallen in een paar weken normaliseert.9
Meestal is er volledig herstel van het hartspierweefsel zonder restverschijnselen, maar bij necrose van het
spierweefsel treedt er verlittekening op.2 8 Complicaties,
zoals ventrikelaritmieën, coronairocclusie, een ventrikelaneurysma of ventrikeldilatatie, zijn zeldzaam en werden enkel in casuïstische publicaties beschreven.10-12
Aangezien in veel gevallen een contusio cordis dus
onopgemerkt blijft, is de prevalentie ervan bij traumapatiënten niet bekend.
Bij patiënt A werd in eerste instantie onderzoek verricht naar de oorzaak van de opmerkelijke dilatatie van
a
b
c
d
figuur 2. Myocardperfusiescintigrafie met technetium-99msestamibi tijdens inspanning (a en c) en in rust (b en d): (a-b):
op de dwarsdoorsneden van de apex naar de basis van het hart
(van links naar rechts) is er sterke asymmetrische activiteitopname van het rechter ventrikel (die bij een normaal hart niet
of nauwelijks zichtbaar zou zijn) met dorsaal hypertrofie (*) en
ventraal een normale ventrikelwand (groene pijl); de afbeelding van het linker ventrikel is normaal; (c-d): op de horizontale langeasdoorsneden (niet anatomisch, maar verkregen door
kantelende bewerking van de digitale gegevens) met de apex
ter hoogte van de pijlpunt, van basaal naar apicaal (van links
naar rechts), is er hypertrofie van de vrije wand van het rechter ventrikel (*), en ventraal/apicaal een normale rechterventrikelwand (groene pijl); de afbeelding van het septum en het
linker ventrikel is normaal.
Oorzaken van rechterventrikeldilatatie13
pulmonale hypertensie
chronisch obstructief longlijden
chronische longembolieën
secundair aan linkerhartfalen
primaire pulmonale hypertensie
pulmonalisklep- en tricuspidalisklepafwijkingen
stenose of insufficiëntie
– congenitaal: ziekte van Ebstein (misvorming van de tricuspidalisklep)
– secundair aan: endocarditis, trauma, reuma, carcinoïd, syndroom van Löffler (eosinofiel infiltraat)
volumeoverbelasting door shunts
atriumseptumdefect
abnormaal inmondende longvenen
andere oorzaken
rechterventrikelinfarct
gedilateerde cardiomyopathie
aritmogene rechterventrikeldysplasie
contusio cordis
het rechter ventrikel (tabel).13 Diverse mogelijke oorzaken konden op basis van het beschreven onderzoek worden uitgesloten. Pas bij een poliklinische controle kwam,
bij een herhaling van de anamnese, het motorongeval
aan het licht, dat, gecombineerd met typische afwijkingen bij het beeldvormend onderzoek, de diagnose ‘contusio cordis’ deed vermoeden. Ten eerste, vanwege zijn
ligging direct achter het borstbeen, wordt bij een contusio cordis vooral het rechter ventrikel frequent beschadigd en is het linker ventrikel relatief veel minder aangedaan1 2 7 8 (figuur 3). Daarnaast was het aneurysma van
de apex van het linker ventrikel, dat eerder beschreven
werd als complicatie na een stomp borstwandtrauma,
richtinggevend.10 Ten tweede toonde het rechter ventrikel bij 99mTc-sestamibiscintigrafie duidelijk een verhoogde activiteitopname (zie figuur 2), welke bevinding bij
afwezigheid van pulmonale hypertensie past bij hypertrofie van de ventrikelwand. De rechterventrikelwand
bleek echter asymmetrisch verdikt, waarbij het tegen het
borstbeen gelegen deel dunner was dan de overige delen
van de hypertrofische ventrikelwand. Dit zou verklaard
kunnen worden door compensatoire hypertrofie van
niet-beschadigde delen, zoals ook gezien wordt bij herstel na een hartinfarct.3 4 Vanwege veranderingen in de
systolische en de diastolische belasting van de ventrikels
treedt er ‘remodeling’ op om een goede ventriculaire
functie te behouden.3 De vroege postinfarctfase wordt
gekenmerkt door dilatatie van de beschadigde delen,
waardoor een ruptuur of een aneurysma kan ontstaan.
In de late fase zijn er globale dilatatie en vormverandering van het ventrikel, met hypertrofie van de onbeschadigde delen van de ventrikelwand.4
De bevindingen bij onze patiënt kwamen dus treffend
overeen met de beschreven postinfarctveranderingen.
Aangezien er geen aanwijzingen waren voor een doorgemaakt infarct, kunnen deze typische afwijkingen naar
Ned Tijdschr Geneeskd 2001 15 december;145(50)
2445
gemaakt infarct, maar met een contusio cordis in zijn
vroege voorgeschiedenis.
rechter
atrium
borstwand
rechter
ventrikel
apex
linker
ventrikel
linker
atrium
echografische
doorsnede
figuur 3. Schematische weergave van een echocardiografische
horizontale doorsnede door de vier hartkamers.13 De frequentst beschadigde delen bij een contusio cordis zijn het ventrale deel van het rechter ventrikel en de apex van het linker
ventrikel.
abstract
An unexplained right ventricle dilation clarified by a cardiac
contusion experienced many years previously. – In a 52-year-old
man with new onset atrial fibrillation, transthoracic echocardiography showed an isolated, considerably dilated right
ventricle. Frequent causes of right ventricular dilatation were
ruled out. The image-forming investigation showed an isolated
dilation of the ventral part of the heart, which, in combination
with a blunt chest trauma 30 years previously, led to a previous
cardiac contusion being suspected. In accordance with this
hypothesis myocardial scintigraphy showed asymmetric hypertrophy of the right ventricular wall, which is consistent with the
remodeling that occurs in response to injured cardiac tissue.
After electrical cardioversion sinus rhythm was obtained; the
patient remained symptom free.
1
onze mening met een contusio cordis worden verklaard.
Vanwege het gebrek aan medische gegevens van het
motorongeval kan een tricuspidalisklepinsufficiëntie als
initiële oorzaak niet met zekerheid worden uitgesloten.
Een tricuspidalisklepinsufficiëntie, wanneer langdurig
bestaand, kan namelijk ook een forse rechterventrikeldilatatie geven.10 De TTE evenals de TEE toonde echter geen structurele of functionele afwijkingen van de
tricuspidalisklep, waardoor een primaire tricuspidalisklepafwijking minder waarschijnlijk werd geacht.
De relatie tussen het boezemfibrilleren en de doorgemaakte contusio cordis kon overigens verklaard worden
door de enorme dilatatie van het rechter ventrikel met
een uitgerekte tricuspidalisklepring. Door de tricuspidalisinsufficiëntie werd de druk in de rechter boezem verhoogd, waardoor dilatatie, aritmogene veranderingen
van het boezemweefsel en uiteindelijk boezemfibrilleren ontstonden.13
2
3
4
5
6
7
8
9
10
conclusie
Contusio cordis is een aandoening die meestal onopgemerkt verloopt met een volledig herstel van het hartspierweefsel. Dit herstel gaat vanwege veranderde belasting gepaard met structurele veranderingen van het
ventrikel, zoals dilatatie, vormverandering en compensatoire hypertrofie. Deze ‘remodeling’ is gedetailleerd
beschreven na een hartinfarct. Wij beschreven een patiënt met gelijke tekenen van ‘remodeling’ zonder door-
2446
Ned Tijdschr Geneeskd 2001 15 december;145(50)
11
12
13
literatuur
Frazee RC, Mucha P, Farnell MB, Miller FA. Objective evaluation
of blunt cardiac trauma. J Trauma 1986;26:510-20.
Tenzer ML. The spectrum of myocardial contusion: a review. J
Trauma 1985;25:620-7.
Bolognese L, Cerisano G. Early predictors of left ventricular remodeling after acute myocardial infarction. Am Heart J 1999;138
(2 Pt 2):S79-83.
Sutton MG, Sharpe N. Left ventricular remodeling after myocardial infarction. Circulation 2000;101:2981-8.
Banning AP, Pillai R. Non-penetrating cardiac and aortic trauma.
Heart 1997;78:226-9.
Adams III JE, Davila-Roman VG, Bessey PQ, Blake DP, Ladenson
JH, Jaffe AS. Improved detection of cardiac contusion with cardiac
troponin I. Am Heart J 1996;131:308-12.
Weiss RL, Brier JA, O’Connor W, Ross S, Brathwaite CM. The usefulness of transesophageal echocardiography in diagnosing cardiac
contusions. Chest 1996;109:73-7.
Schamp DJ, Plotnick GD, Croteau D, Rosenbaum RC, Johnston
GS, Rodriguez A. Clinical significance of radionuclide angiographically-determined abnormalities following acute blunt chest trauma.
Am Heart J 1988;116(2 Pt 1):500-4.
Sutherland GR, Cheung HW, Holliday RL, Driedger AA, Sibbald
WJ. Hemodynamic adaptation to acute myocardial contusion complicating blunt chest injury. Am J Cardiol 1986;57:291-7.
Stone DL, Fleming HA. Aneurysm of left ventricle and left coronary
artery after non-penetrating chest trauma. Br Heart J 1983;50:495-7.
Fox KM, Rowland E, Krikler DM, Bentall HH, Goodwin JF.
Electrophysiological manifestations of non-penetrating cardiac
trauma. Br Heart J 1980;43:458-62.
Wadhwa SS, Mansberg R, Fernandes VB. Old traumatic ventricular
septal defect seen on myocardial perfusion imaging. Clin Nucl Med
1999;24:135.
Braunwald E. Heart disease. A textbook of cardiovascular medicine.
5th ed. Philadelphia: Saunders; 1997.
Aanvaard op 25 juli 2001